Hvilket par Hvad har det samme antal valenselektroner magnesium og kalium lithium calcium argon xenon fosfor tellurium?
Forståelse af valenselektroner
Valenselektroner er elektronerne i det yderste energiniveau af et atom. Dette er de elektroner, der er involveret i kemisk binding.
Periodiske tendenser
* gruppe (kolonne): Elementer inden for den samme gruppe (kolonne) i den periodiske tabel har det samme antal valenselektroner.
* perioder (rækker): Antallet af valenselektroner øges generelt, når du bevæger dig over en periode (række) fra venstre mod højre.
analyse af elementerne
Lad os nedbryde hvert element:
* magnesium (mg): Gruppe 2, 2 valenselektroner
* kalium (k): Gruppe 1, 1 valenselektron
* lithium (Li): Gruppe 1, 1 valenselektron
* calcium (CA): Gruppe 2, 2 valenselektroner
* argon (AR): Gruppe 18 (ædelgas), 8 valenselektroner
* Xenon (XE): Gruppe 18 (ædelgas), 8 valenselektroner
* fosfor (p): Gruppe 15, 5 valenselektroner
* tellurium (TE): Gruppe 16, 6 Valenselektroner
par med det samme antal valenselektroner
* magnesium (mg) og calcium (CA): Begge har 2 valenselektroner.
* kalium (k) og lithium (LI): Begge har 1 valenselektron.
* argon (AR) og Xenon (XE): Begge har 8 valenselektroner (fuld ydre skal).
Bemærk: Antallet af valenselektroner er en nøglefaktor, der bestemmer et elements kemiske opførsel.
Sidste artikelHvad er pH for polsk remover?
Næste artikelHvad er pH for Softdrink (farveløs)?
 Varme artikler
Varme artikler
-
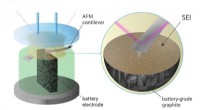 Forskere får et smugkig på en nøgleproces i batterilevetidenEn hovedoversigt over eksperimentet. Kredit:Pavel Odinev / Skoltech Forskere fra Skoltech Center for Energividenskab og Teknologi (CEST) visualiserede dannelsen af en fast elektrolyt-interfase p
Forskere får et smugkig på en nøgleproces i batterilevetidenEn hovedoversigt over eksperimentet. Kredit:Pavel Odinev / Skoltech Forskere fra Skoltech Center for Energividenskab og Teknologi (CEST) visualiserede dannelsen af en fast elektrolyt-interfase p -
 Lys forbrænder med nye syrerLysbestråling på den omgivende inerte nye PLAG genererer Lewis Acid som en alsidig katalysator. Som billedet viser, er denne proces som at vende et kortspil og altid komme med det helt mægtige kort. K
Lys forbrænder med nye syrerLysbestråling på den omgivende inerte nye PLAG genererer Lewis Acid som en alsidig katalysator. Som billedet viser, er denne proces som at vende et kortspil og altid komme med det helt mægtige kort. K -
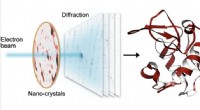 Sniger op på små krystaller med elektrondiffraktionVed seriel elektrondiffraktion, en lille elektronstråle rammer sekventielt tusindvis af små krystaller lavet af proteiner, som spreder strålen i diffraktionsmønstre. Fra disse mønstre, strukturen af
Sniger op på små krystaller med elektrondiffraktionVed seriel elektrondiffraktion, en lille elektronstråle rammer sekventielt tusindvis af små krystaller lavet af proteiner, som spreder strålen i diffraktionsmønstre. Fra disse mønstre, strukturen af -
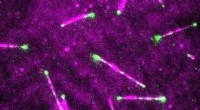 Ser et lægemiddel i aktion:Præcis handling mod kræftmedicin i cellen afklaretMikrotubuli med fluorescerende markører ved spidserne, in vitro. Kredit:Ankit Rai, Utrecht Universitet. Forskere fra Utrecht University har anvendt avanceret mikroskopi for at visualisere aktivite
Ser et lægemiddel i aktion:Præcis handling mod kræftmedicin i cellen afklaretMikrotubuli med fluorescerende markører ved spidserne, in vitro. Kredit:Ankit Rai, Utrecht Universitet. Forskere fra Utrecht University har anvendt avanceret mikroskopi for at visualisere aktivite
- En ny rapport opsummerer, hvordan klimaændringer påvirker vandkredsløbet i Tyskland
- Hvordan opfindelsen af mikroskop. Hjælp videnskabsmænd med at forstå celler?
- Kan fiske skolebiler i hvordan man kører sammen?
- En alsidig højfølsom overfladespændingsmembransensor
- Hvordan virker en Fresnel-linse? Magien bag glasset
- Hvad er den nordligste breddegrad?


