Når en væske og dens damp er ved ligevægtstryk, nedsættes pludselig afkøling hvorfor?
Forståelse af ligevægt
* ligevægt: Når en væske og dens damp er i ligevægt, er fordampningshastigheden (væske til gas) lig med kondensationshastigheden (gas til væske). Dette betyder, at der er en konstant udveksling af molekyler mellem væske- og dampfaserne, men de samlede beløb forbliver de samme.
* damptryk: Det tryk, der udøves af dampen i ligevægt med væsken, kaldes damptrykket. Det er et mål for, hvor let væsken fordamper.
Effekten af trykreduktion
1. skiftende ligevægt: Når du pludselig reducerer trykket over væsken, forstyrres ligevægten. Damptrykket er nu højere end det ydre tryk.
2. Øget fordampning: Denne trykubalance tilskynder flere molekyler til at flygte fra den flydende fase ind i dampfasen for at forsøge at nå en ny ligevægt. Dette skyldes, at de flydende molekyler nu er under mindre pres fra den omgivende atmosfære.
3. Energiabsorption: Fordampning er en endotermisk proces. Det kræver energi for at bryde de intermolekylære bindinger, der holder væskemolekylerne sammen. Denne energi absorberes fra den omgivende væske, hvilket fører til et fald i dens temperatur.
Køleeffekten
Nettoeffekten er, at væsken afkøles, da den absorberer energi for at understøtte den øgede fordampningshastighed. Dette skyldes, at væsken mister energi til dampfasen, når den prøver at genoprette ligevægt ved det lavere tryk.
Eksempel:
Forestil dig en forseglet beholder med vand- og vanddamp i ligevægt. Hvis du pludselig åbner beholderen, falder trykket over vandet. Vandet vil begynde at fordampe hurtigt, tage varmen væk fra den resterende væske og få det til at køle ned.
Nøglepunkt: Denne køleeffekt er et grundlæggende princip, der bruges i processer som køling og aircondition.
 Varme artikler
Varme artikler
-
 Kraftværker drevet af lysKredit:CC0 Public Domain Grønne planter, alger og nogle bakterier bruger sollys til at omdanne energi. Pigmenterne i klorofyl absorberer elektromagnetisk stråling, som fremkalder kemiske reaktione
Kraftværker drevet af lysKredit:CC0 Public Domain Grønne planter, alger og nogle bakterier bruger sollys til at omdanne energi. Pigmenterne i klorofyl absorberer elektromagnetisk stråling, som fremkalder kemiske reaktione -
 Forskere foreslår at bruge pindsvin-lignende partikler til at fremskynde cellebiokemiske reaktionerUrchin-lignende partikler rettet af et magnetfelt. Kredit:Dmitry Lisovsky Forskning fra ITMO foreslår at bruge urchin-lignende partikler styret af et magnetfelt til at fremskynde kemiske reaktione
Forskere foreslår at bruge pindsvin-lignende partikler til at fremskynde cellebiokemiske reaktionerUrchin-lignende partikler rettet af et magnetfelt. Kredit:Dmitry Lisovsky Forskning fra ITMO foreslår at bruge urchin-lignende partikler styret af et magnetfelt til at fremskynde kemiske reaktione -
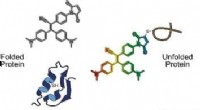 Molekylær sondekort forkert foldet proteometilstand i levende cellerKredit:Wiley Proteinernes foldningstilstand i levende celler afspejler ofte cellens generelle helbred. Australske forskere har udviklet en molekylær sonde, der registrerer proteometilstanden - hel
Molekylær sondekort forkert foldet proteometilstand i levende cellerKredit:Wiley Proteinernes foldningstilstand i levende celler afspejler ofte cellens generelle helbred. Australske forskere har udviklet en molekylær sonde, der registrerer proteometilstanden - hel -
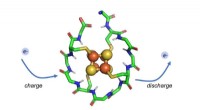 Forskere identificerer protein, der kan have eksisteret, da livet begyndteForskere har designet et syntetisk lille protein, der ombrydes omkring en metalkerne sammensat af jern og svovl. Dette protein kan gentagne gange oplades og udledes, gør det muligt for den at transpor
Forskere identificerer protein, der kan have eksisteret, da livet begyndteForskere har designet et syntetisk lille protein, der ombrydes omkring en metalkerne sammensat af jern og svovl. Dette protein kan gentagne gange oplades og udledes, gør det muligt for den at transpor
- Forskelle mellem en vindvane og en anemometer
- Ny AI kan opdage urinvejsinfektioner
- Sidste vinter Detroit auto viser en skygge af sit tidligere jeg
- Bekræftet:I rummet kan ingen høre dig skrige
- Hvordan er svampe forme og gær forskellige?
- USA lancerer undersøgelse af Frances planlagte skat til giganter


