Diffunderer lettere gaspartikler mindre hurtigt end tungere partikler?
* kinetisk molekylær teori: Denne teori siger, at gaspartikler er i konstant tilfældig bevægelse. Den gennemsnitlige kinetiske energi for disse partikler er direkte proportional med den absolutte temperatur.
* Gennemsnitlig hastighed: Lysere partikler ved den samme temperatur har en højere gennemsnitlig hastighed end tungere partikler. Dette skyldes, at kinetisk energi (KE) er givet af KE =1/2 * mv², hvor M er masse og V er hastighed. For den samme KE skal en lettere partikel have en højere hastighed.
* diffusion: Diffusion er processen med partikler, der spreder sig fra et område med høj koncentration til et område med lav koncentration. Jo hurtigere partiklerne bevæger sig, jo hurtigere spreder de sig.
Derfor diffunderer lettere gaspartikler hurtigere på grund af deres højere gennemsnitlige hastighed.
 Varme artikler
Varme artikler
-
 Dette service lavet af sukkerrør og bambus nedbrydes på 60 dageEn kvinde, der håndterer service lavet af bambus og affald fra fødevareindustrien. Kredit:Ruby Wallau/Northeastern University Forskere har designet et sæt grønt service lavet af sukkerrør og bambu
Dette service lavet af sukkerrør og bambus nedbrydes på 60 dageEn kvinde, der håndterer service lavet af bambus og affald fra fødevareindustrien. Kredit:Ruby Wallau/Northeastern University Forskere har designet et sæt grønt service lavet af sukkerrør og bambu -
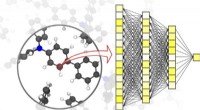 Maskinlæring fremskynder simuleringer inden for materialevidenskabNeurale netværk muliggør præcise simuleringer inden for materialevidenskab – ned til niveauet af individuelle atomer. Kredit:Pascal Friedrich, SÆT Forskning, udvikling, og produktion af nye materi
Maskinlæring fremskynder simuleringer inden for materialevidenskabNeurale netværk muliggør præcise simuleringer inden for materialevidenskab – ned til niveauet af individuelle atomer. Kredit:Pascal Friedrich, SÆT Forskning, udvikling, og produktion af nye materi -
 Fremtrædende akademikere efterlyser mere videnskab inden for retsmedicinSalk neuroforsker Thomas Albright studerer syn og hukommelse. Kredit:Salk Instituttet Da retsvidenskaben står over for stigende kontrol, da den spiller en stadig mere fremtrædende rolle i retsplej
Fremtrædende akademikere efterlyser mere videnskab inden for retsmedicinSalk neuroforsker Thomas Albright studerer syn og hukommelse. Kredit:Salk Instituttet Da retsvidenskaben står over for stigende kontrol, da den spiller en stadig mere fremtrædende rolle i retsplej -
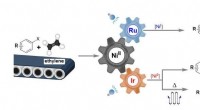 Katalytisk omdannelse af ethylenIllustration, der viser de nikkelkatalyserede reaktioner mellem kommercielt tilgængeligt arylhalogenid og ethylen. Oxidationstilstanden af nikkelkatalysatoren ændres til +1 eller 0, når den modulere
Katalytisk omdannelse af ethylenIllustration, der viser de nikkelkatalyserede reaktioner mellem kommercielt tilgængeligt arylhalogenid og ethylen. Oxidationstilstanden af nikkelkatalysatoren ændres til +1 eller 0, når den modulere
- Hvorfor Olie vil ikke blande i vand?
- Fotoforfalskning fanget via overlisteteknikker
- Hvad kan man konkludere om jorden i Odysseen?
- Dommedagsuret sidder fast på 100 sekunder til midnat
- Silicon Valley-mysteriet:Hvorfor 'tiden er inde' for Eric Schmidt at forlade som Alphabet-formand
- Kontaktløs 3-D fingeraftryksidentifikation


