Hvad er isomotisk løsning?
Her er en sammenbrud:
* osmotisk tryk: Det tryk, der skal påføres en opløsning for at forhindre den indre strøm af vand på tværs af en semipermeabel membran.
* semipermeabel membran: En membran, der tillader nogle molekyler at passere, men ikke andre.
* isotonisk: Et udtryk, der ofte bruges ombytteligt med isomotisk, men det henviser specifikt til samme koncentration af opløste stoffer .
Hvorfor er dette vigtigt?
Forståelse af isomotiske løsninger er afgørende i biologiske systemer, især i:
* cellulær funktion: Celler er omgivet af en semipermeabel membran. Hvis det omgivende miljø er isomotisk for cellens interne miljø, er der ingen nettobevægelse af vand i eller ud af cellen. Dette opretholder cellevolumen og -funktion.
* Medicinske behandlinger: Intravenøse væsker er designet til at være isomotisk for blodplasma, hvilket forhindrer skade på røde blodlegemer og opretholder korrekt væskebalance i kroppen.
Eksempler på isomotiske løsninger:
* Normal saltvand (0,9% NaCl): Isomotisk for humant blodplasma.
* Lacterated Ringer's løsning: Isomotisk for humant blodplasma.
* to opløsninger med den samme koncentration af opløste stoffer: For eksempel er en 1M glukoseopløsning og en 1M saccharoseopløsning isomotisk.
Vigtig note: Mens isotonisk og isomotisk ofte bruges om hverandre, er der en subtil forskel. isotonisk Henviser specifikt til * koncentrationen * af opløste stoffer, mens isomotisk henviser til det *osmotiske tryk *. I nogle tilfælde kan opløsninger have det samme osmotiske tryk, men forskellige opløste koncentrationer, såsom opløsninger, der indeholder forskellige typer opløste stoffer.
Sidste artikelForklar den aktuelle fordeling tynde tråd anteena detaljeret?
Næste artikelHvad sker der, hvis og saltopløsninger er blandet?
 Varme artikler
Varme artikler
-
 Det perfekte shot af espresso hver gang med kemiForfining af espressobrygningsprocessen kan resultere i sparede penge og konsekvent velsmagende kaffe. Kredit:Charlie Litchfield, University of Oregon Den gennemsnitlige amerikaner drikker mere en
Det perfekte shot af espresso hver gang med kemiForfining af espressobrygningsprocessen kan resultere i sparede penge og konsekvent velsmagende kaffe. Kredit:Charlie Litchfield, University of Oregon Den gennemsnitlige amerikaner drikker mere en -
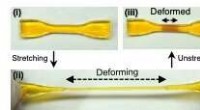 Selvvoksende materialer, der styrker som reaktion på kraftEn dobbeltnetværkshydrogel (i). Efter strækning (ii), skøre sektioner går i stykker, tillader en generation af mekanoradikale stoffer, angivet ved farveændring (iii). Kredit:Gong J.P. et al., Mekanore
Selvvoksende materialer, der styrker som reaktion på kraftEn dobbeltnetværkshydrogel (i). Efter strækning (ii), skøre sektioner går i stykker, tillader en generation af mekanoradikale stoffer, angivet ved farveændring (iii). Kredit:Gong J.P. et al., Mekanore -
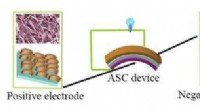 FeCo-selenid - et muligt næste generations materiale til energilagringsenhederDet skematiske fremstillingsdiagram af FeCo-selenid//Fe 2 O 3 asymmetrisk superkondensator (ASC). FeCo-seleniden og Fe 2 O 3 elektroder fungerer som henholdsvis positive og negative elektroder
FeCo-selenid - et muligt næste generations materiale til energilagringsenhederDet skematiske fremstillingsdiagram af FeCo-selenid//Fe 2 O 3 asymmetrisk superkondensator (ASC). FeCo-seleniden og Fe 2 O 3 elektroder fungerer som henholdsvis positive og negative elektroder -
 Serendipity udvider mulighederne for fremstilling af grafitKredit:CC0 Public Domain Forskere fra Curtin University har uventet opdaget en ny måde at lave krystallinsk grafit, et væsentligt materiale, der bruges til fremstilling af lithium-ion-batterier.
Serendipity udvider mulighederne for fremstilling af grafitKredit:CC0 Public Domain Forskere fra Curtin University har uventet opdaget en ny måde at lave krystallinsk grafit, et væsentligt materiale, der bruges til fremstilling af lithium-ion-batterier.
- Opstart retter sig mod døsig kørsel med næste generations førersikkerhedssystem
- Hackere lækker fransk hospitalspatientdata i løsesumskamp
- Deltager aquaporiner i aktiv transport en celle?
- Nyt selvsamlet monolag er modstandsdygtigt over for luft
- Hvad er størrelsessammenligningen af Saturn og Merkur?
- Lys i mørke:Et eksperimentelt kig på palæolitisk hulebelysning


