Hvad er den korrekte placering af brint i periodisk tabel?
* gruppe 1 (alkalimetaller): Hydrogen har et elektron i sin yderste skal, svarende til alkalimetaller. Det kan miste dette elektron for at danne en positiv ion (H+).
* gruppe 17 (halogener): Hydrogen kan også få et elektron til dannelse af en negativ ion (H-), svarende til halogenerne.
Så hvor hører det til?
* Historisk: Hydrogen blev ofte anbragt over lithium i gruppe 1 på grund af dets tendens til at miste et elektron.
* Moderne syn: På grund af sin evne til at få et elektron også, er Hydrogens egenskaber ikke perfekt i overensstemmelse med hverken gruppe 1 eller gruppe 17. Det står ofte alene øverst på den periodiske tabel.
Den mest almindelige måde at skildre brint på er:
* over tabellen: Dette betyder dens unikke natur, og at den ikke passer pænt ind i nogen specifik gruppe.
Key Takeaway: Hydrogen er et specielt element med egenskaber, der overlapper hinanden med både alkalimetaller og halogener, hvilket gør dens placering i den periodiske tabel til en gang om løbende debat.
 Varme artikler
Varme artikler
-
 Strækbare og klemme bløde sensorer et skridt nærmere takket være den nye bindingsmetodeEn sensor holdt mellem to fingre. Kredit:Michael Kasimatis Bioingeniører fra Imperial College London har fundet en måde at skabe elastiske og squeezy bløde sensorenheder ved at binde gummi til ele
Strækbare og klemme bløde sensorer et skridt nærmere takket være den nye bindingsmetodeEn sensor holdt mellem to fingre. Kredit:Michael Kasimatis Bioingeniører fra Imperial College London har fundet en måde at skabe elastiske og squeezy bløde sensorenheder ved at binde gummi til ele -
 Ny deaktiveringsmekanisme for switchproteiner fundetKlaus Gerwert, Till Rudack og Carsten Kötting (fra venstre) har undersøgt switch -proteiner i årevis, for eksempel Ras -proteinet afbildet her. Kredit:RUB En ny mekanisme til deaktivering af switc
Ny deaktiveringsmekanisme for switchproteiner fundetKlaus Gerwert, Till Rudack og Carsten Kötting (fra venstre) har undersøgt switch -proteiner i årevis, for eksempel Ras -proteinet afbildet her. Kredit:RUB En ny mekanisme til deaktivering af switc -
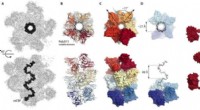 Forskere tager billeder af antistoffer, der arbejder sammen mod malariaDisse tal fra den nye Videnskabens fremskridt papir viser, hvordan antistoffer binder sammen for at låse malarias circumsporozoit-protein i en spiralkonformation. Kredit:Wilson/Ward labs, Scripps Re
Forskere tager billeder af antistoffer, der arbejder sammen mod malariaDisse tal fra den nye Videnskabens fremskridt papir viser, hvordan antistoffer binder sammen for at låse malarias circumsporozoit-protein i en spiralkonformation. Kredit:Wilson/Ward labs, Scripps Re -
 Traditionel eutektisk legering bringer nyt håb til metal-oxygenbatterier med høj energi densiteta) Sammenligning af oxidation og korrosionsbestandighed af Li-Na eutektisk legering og Na-metal. SEM-billeder til Li-Na-legering b), og Na c) elektroder efter fem stripping/pletteringscyklusser. d) Sp
Traditionel eutektisk legering bringer nyt håb til metal-oxygenbatterier med høj energi densiteta) Sammenligning af oxidation og korrosionsbestandighed af Li-Na eutektisk legering og Na-metal. SEM-billeder til Li-Na-legering b), og Na c) elektroder efter fem stripping/pletteringscyklusser. d) Sp
- Hvad sker der i de første øjeblikke af dannelse af sommerfugleskæl
- Chitosan belagt, kemoterapipakkede nanopartikler kan målrette mod kræftstamceller
- En stjernernes indtrængers indvirkning på vores solsystem
- Flere minoriteter mærkede indlæringshandicap på grund af sociale uligheder, undersøgelse finder
- Billede:Solens tilbagevenden ved Antarcticas Concordia forskningsstation
- Forskere skaber en super antioxidant:Almindelig katalysator ceriumoxid åbner døren til nanokemi fo…


