Hvor mange gram vand er nødvendige for at reagere med 74,0 g cacn2?
1. Skriv den afbalancerede kemiske ligning:
CACN₂ (S) + 3H₂O (L) → Caco₃ (S) + 2NH₃ (G)
2. Beregn den molære masse af Cacn₂ og H₂O:
* Cacn₂:40,08 g/mol (Ca) + 12,01 g/mol (c) + 2 * 14,01 g/mol (n) =80,10 g/mol
* H₂O:2 * 1,01 g/mol (H) + 16,00 g/mol (O) =18,02 g/mol
3. Konverter gram Cacn₂ til mol:
* mol CACN₂ =74,0 g / 80,10 g / mol =0,924 mol
4. Brug molforholdet fra den afbalancerede ligning til at finde mol af H₂O:
* Ligningen viser, at 1 mol cacn₂ reagerer med 3 mol H₂O.
* mol H₂O =0,924 mol cacn₂ * (3 mol H₂O / 1 mol cacn₂) =2,772 mol H₂O
5. Konverter mol H₂O til gram:
* gram H₂O =2,772 mol * 18,02 g/mol =50,0 g
Derfor er der behov for 50,0 gram vand for at reagere med 74,0 gram cacn₂.
Sidste artikelHvordan forbereder du 1 molær tris?
Næste artikelBordsalt er resultatet af?
 Varme artikler
Varme artikler
-
 Efterladt korn fra bryggerier kunne omdannes til brændsel til boligerKredit:CC0 Public Domain En forsker fra Queens University Belfast har udviklet en billig teknik til at omdanne rester af byg fra alkoholbryggerier til kulstof, som kunne bruges som vedvarende bræn
Efterladt korn fra bryggerier kunne omdannes til brændsel til boligerKredit:CC0 Public Domain En forsker fra Queens University Belfast har udviklet en billig teknik til at omdanne rester af byg fra alkoholbryggerier til kulstof, som kunne bruges som vedvarende bræn -
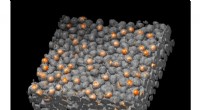 Den mest komplette undersøgelse af batterifejl ser lysetForskere har skabt en ny teknik, der scanner tusindvis af partikler i elektroden på et batteri på én gang. Målet er at forstå, hvordan revner i disse partikler påvirker batteriets ydeevne, så industri
Den mest komplette undersøgelse af batterifejl ser lysetForskere har skabt en ny teknik, der scanner tusindvis af partikler i elektroden på et batteri på én gang. Målet er at forstå, hvordan revner i disse partikler påvirker batteriets ydeevne, så industri -
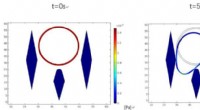 Små filtre hjælper med at opdage kræftblodcellerSimuleringer, der viser cancerøse myelomceller, også kendt som cCPCer, sidde fast mellem mikrosøjler i en ny filterenhed, beskrevet i Biomicrofluidics. Blå kontur er cCPCen, og væsken strømmer fra top
Små filtre hjælper med at opdage kræftblodcellerSimuleringer, der viser cancerøse myelomceller, også kendt som cCPCer, sidde fast mellem mikrosøjler i en ny filterenhed, beskrevet i Biomicrofluidics. Blå kontur er cCPCen, og væsken strømmer fra top -
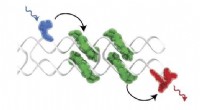 Lær af fotosyntese:Syntetiske kredsløb kan høste lysenergiSet i gråt, DNA DX-flisen danner et stillads, der muliggør en præcis placering af farvestofmolekyle kromoforer, som samler sig selv på stilladset i karakteristiske J-konfigurationer, ses i grønt. Blå
Lær af fotosyntese:Syntetiske kredsløb kan høste lysenergiSet i gråt, DNA DX-flisen danner et stillads, der muliggør en præcis placering af farvestofmolekyle kromoforer, som samler sig selv på stilladset i karakteristiske J-konfigurationer, ses i grønt. Blå
- Fremskridt inden for lysfiltreringsteknologi har konsekvenser for LCD-skærme, lasere og mere
- Hvad får en isolator til at isolere?
- Er erosion bevægelsen af forvitret sten og jord sand eller falsk?
- Hvilken proces opstår, når DNA'et for et gen fremstiller et mRNA -molekyle?
- Hvad er en atomreaktor, og hvad er dens formål?
- Hvad er betydningen og betydningen af en blodmåneformørkelse?


