Hvordan kan omkrystallisation adskille en blanding?
Princippet:
Omkrystallisation er afhængig af forskellen i opløselighed af den ønskede forbindelse og urenheder i et valgt opløsningsmiddel. Den grundlæggende idé er:
* opløselighed: De fleste faste stoffer opløses lettere ved højere temperaturer.
* Krystallisation: Når opløsningen afkøles, falder opløseligheden af den ønskede forbindelse, hvilket får den til at krystallisere ud af opløsningen og efterlader urenheder.
Processen:
1. opløste: Den uren faste blanding opløses i et varmt opløsningsmiddel (normalt det minimale beløb, der er nødvendigt for fuldstændig opløsning). Valget af opløsningsmiddel er afgørende - det skal:
* Opløs den ønskede forbindelse godt, når den er varm.
* Opløs urenheder dårligt eller slet ikke, selv når de er varmt.
2. Filtrering af varmt: Mens det er varmt, filtreres opløsningen for at fjerne eventuelle uopløselige urenheder. Dette gøres hurtigt for at forhindre for tidlig krystallisation.
3. afkøling og krystallisation: Opløsningen afkøles langsomt, hvilket giver den ønskede forbindelse mulighed for at krystallisere, når opløseligheden falder.
4. Filtrering af kulde: Når de er afkølet, filtreres krystallerne for at adskille dem fra den resterende opløsning (indeholdende de opløste urenheder).
5. vask og tørring: Krystallerne vaskes med en lille mængde koldt opløsningsmiddel for at fjerne eventuelle resterende urenheder og tørres derefter for at fjerne ethvert resterende opløsningsmiddel.
Nøglepunkter:
* Valg af opløsningsmiddel: Nøglen til vellykket omkrystallisation er at vælge et opløsningsmiddel, der har en stor forskel i opløselighed for den ønskede forbindelse ved høje og lave temperaturer.
* langsom afkøling: Langsom afkøling muliggør dannelse af større, renere krystaller.
* urenheder: Urenheder, der opløses let i opløsningsmidlet, forbliver i opløsningen, mens de, der er uopløselige, fjernes under den indledende varme filtrering.
* Flere omkrystallisationer: Nogle gange er en enkelt omkrystallisation muligvis ikke nok til at opnå høj renhed. Flere omkrystallisationstrin kan yderligere øge renheden.
Eksempel:
Lad os sige, at du har en blanding af salt (NaCl) og sukker (C12H22O11). Du kan adskille dem ved hjælp af omkrystallisation.
* opløsningsmiddel: Vand er et godt valg. Salt er meget opløseligt i vand, både varmt og koldt. Sukker er meget mere opløseligt i varmt vand end koldt vand.
* opløste: Opløs blandingen i varmt vand.
* filtrering af varmt: Fjern eventuelle uopløselige urenheder (hvis de er til stede).
* afkøling: Når opløsningen afkøles, krystalliserer sukker og lader saltet være opløst i vandet.
* Filtrering af kulde: Saml sukkerkrystallerne og vask dem med koldt vand for at fjerne ethvert resterende salt.
Ansøgninger:
Omkrystallisation er en meget anvendt teknik inden for kemi og relaterede felter, herunder:
* oprensning af forbindelser: Det er vigtigt for at rense organiske forbindelser, farmaceutiske stoffer og andre kemikalier.
* Opnåelse af rene krystaller: Krystaller opnået gennem omkrystallisation bruges ofte i forskning, materialevidenskab og andre felter.
Fortæl mig, hvis du har andre spørgsmål!
 Varme artikler
Varme artikler
-
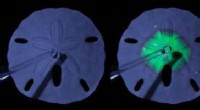 Fra søpindsvinskelet til solcellerDenne billedserie viser et skelet med sanddollar, der gradvist konverterer til en lysemitterende perovskit. Snapshots af denne konvertering er taget på 0s, 5s, 15erne, og 40erne. Kredit:Noorduin Lab,
Fra søpindsvinskelet til solcellerDenne billedserie viser et skelet med sanddollar, der gradvist konverterer til en lysemitterende perovskit. Snapshots af denne konvertering er taget på 0s, 5s, 15erne, og 40erne. Kredit:Noorduin Lab, -
 Ikke-giftigt undervandsklæbemiddel kan bringe ny kirurgisk limPurdue University lektor Julie Liu, til venstre, og doktorand Sydney Hollingshead, forberede sig på at teste et nyt proteinbaseret klæbemiddel under vandet. Kredit:Purdue University image/Erin Easterl
Ikke-giftigt undervandsklæbemiddel kan bringe ny kirurgisk limPurdue University lektor Julie Liu, til venstre, og doktorand Sydney Hollingshead, forberede sig på at teste et nyt proteinbaseret klæbemiddel under vandet. Kredit:Purdue University image/Erin Easterl -
 Brug af en blød krystal til at visualisere, hvordan absorberet kuldioxid opfører sig i væskeDen CO2-absorberende bløde krystal udviklet til denne undersøgelse. Kredit:Shin-ichiro Noro Et team af forskere er lykkedes med at visualisere, hvordan kuldioxid (CO 2 ) opfører sig i en ionisk
Brug af en blød krystal til at visualisere, hvordan absorberet kuldioxid opfører sig i væskeDen CO2-absorberende bløde krystal udviklet til denne undersøgelse. Kredit:Shin-ichiro Noro Et team af forskere er lykkedes med at visualisere, hvordan kuldioxid (CO 2 ) opfører sig i en ionisk -
 Elastisk polymer, der er både stiv og hård, løser mangeårige problemerEn stærkt sammenfiltret hydrogel (venstre) og en almindelig hydrogel (højre). Kredit:Suo Lab/Harvard SEAS Polymer science har muliggjort gummidæk, Teflon og Kevlar, vandflasker i plast, nylonjakke
Elastisk polymer, der er både stiv og hård, løser mangeårige problemerEn stærkt sammenfiltret hydrogel (venstre) og en almindelig hydrogel (højre). Kredit:Suo Lab/Harvard SEAS Polymer science har muliggjort gummidæk, Teflon og Kevlar, vandflasker i plast, nylonjakke
- Får eller taber helium elektroner for at danne forbindelser?
- Mere nøjagtig biopsi ved augmented reality
- En ny type hybridkolloide kvanteprikker/organiske solceller
- Skoler skal tilskynde til bredere deltagelse i naturfagslæring uden for klasseværelset
- Forskel mellem 316 og 308 rustfrit stål
- Hvor får elektromagneter i vandkraftværker deres elektricitet?


