Hvad er forskellen mellem calciumcarbonat og bicarbonat?
calciumcarbonat (caco₃)
* struktur: En fast forbindelse sammensat af et calciumatom, et carbonatom og tre iltatomer.
* egenskaber:
* Hvid, pulveriseret fast stof.
* Uopløselig i vand.
* Fundet naturligt i mineraler som kalksten, kridt og marmor.
* anvendelser:
* Antacid (neutraliserer mavesyre)
* Diættilskud (calciumkilde)
* Byggemateriale (cement, beton)
* Landbrugskalk (jordændring)
calciumbicarbonat (CA (HCO₃) ₂)
* struktur: En forbindelse indeholdende en calciumion (Ca²⁺) og to bicarbonationer (HCO₃⁻).
* egenskaber:
* Findes ikke i solid form.
* Eksisterer kun i opløsning, dannet, når kuldioxid opløses i vand, der indeholder calciumioner.
* Bryder sammen i calciumcarbonat, vand og kuldioxid.
* anvendelser:
* Fundet i grundvand, der bidrager til hårdt vand.
* Involveret i dannelsen af stalaktitter og stalagmitter.
Nøgleforskelle:
* opløselighed: Calciumcarbonat er uopløseligt i vand, mens calciumbicarbonat kun findes i opløsning.
* stabilitet: Calciumbicarbonat er ustabil og nedbrydes let, mens calciumcarbonat er relativt stabil.
* forekomst: Calciumcarbonat findes i fast form i naturen, mens calciumbicarbonat primært findes opløst i vand.
Vigtig note:
Mens calciumcarbonat er et almindeligt mineral, er det vigtigt at bemærke, at calciumbicarbonat ikke er en stabil fast forbindelse. Det findes kun i vandige opløsninger og nedbrydes let til andre forbindelser.
Sidste artikelHvad er det sammensatte navn på Moi2?
Næste artikelHvorfor er polære molekyler ikke i stand til at gå over, medmindre?
 Varme artikler
Varme artikler
-
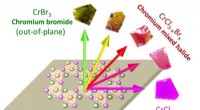 Blandet halogenidkemi kan bruges til at kontrollere magnetisme i ultratynde magnetiske enhederChromchlorid og chrombromid var tidligere kendt som overgangsmetalhalogenider med magnetisering i planet og ud af planet. Boston College-forskere har opdaget en måde at fremstille blandede halogenider
Blandet halogenidkemi kan bruges til at kontrollere magnetisme i ultratynde magnetiske enhederChromchlorid og chrombromid var tidligere kendt som overgangsmetalhalogenider med magnetisering i planet og ud af planet. Boston College-forskere har opdaget en måde at fremstille blandede halogenider -
 Video:Hvordan regner det plastik ?!Kredit:The American Chemical Society Hvert år, mere end 1, 000 tons plastikregn ned på nationalparker og vildmarksområder i det vestlige USA I denne uges afsnit, vi taler om, hvor den plast komme
Video:Hvordan regner det plastik ?!Kredit:The American Chemical Society Hvert år, mere end 1, 000 tons plastikregn ned på nationalparker og vildmarksområder i det vestlige USA I denne uges afsnit, vi taler om, hvor den plast komme -
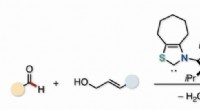 Partnere i katalyse:En effektiv vej til umættede ketonerDen samvirkende virkning af en organokatalysator og en palladiumkatalysator muliggjorde en første dehydrerende direkte allylering mellem aldehyder og allylalkoholer for at producere β, γ-umættede keto
Partnere i katalyse:En effektiv vej til umættede ketonerDen samvirkende virkning af en organokatalysator og en palladiumkatalysator muliggjorde en første dehydrerende direkte allylering mellem aldehyder og allylalkoholer for at producere β, γ-umættede keto -
 Unik kemi - som en dag kan hjælpe med at bekæmpe alvorlig sygdom - fundet i den newzealandske glø…Dr Miriam Sharpe, Institut for Biokemi. Kredit:University of Otago University of Otago forskere i New Zealand har hjulpet med at afdække, hvordan newzealandske glødorme producerer deres glød. En f
Unik kemi - som en dag kan hjælpe med at bekæmpe alvorlig sygdom - fundet i den newzealandske glø…Dr Miriam Sharpe, Institut for Biokemi. Kredit:University of Otago University of Otago forskere i New Zealand har hjulpet med at afdække, hvordan newzealandske glødorme producerer deres glød. En f
- Hvor er alle blomsterne blevet af?
- Indiens TCS krydser en markedsværdi på 100 mia. USD
- Navngiv en renæssance -præstation i hver kategori af matematikarkitektur astronomi og kartografi?
- IBM-forskere efterligner neurons funktionalitet med en faseændringsenhed
- Hvordan produceres ekstra drivhusgasser?
- Hvordan påvirker temperaturstigningen atmosfæren?


