Hvad sker der, når der tilsættes vand til de gaskrukker, hvor svovl blev brændt?
* svovldioxid (SO2) opløses i vand. Svovlforbrænding i luft producerer svovldioxidgas. Denne gas er opløselig i vand, og den reagerer med vandmolekylerne til dannelse af svovlsyre (H2SO3) .
* opløsningen bliver sur. Svovlsyre er en svag syre. Dette betyder, at opløsningen vil have en lavere pH end rent vand, hvilket indikerer surhedsgrad.
* Løsningen vil have en karakteristisk skarp lugt. Sulfurous syre har en skarp, kvælende lugt, som ofte beskrives som ligner brændende kampe.
Kemisk reaktion:
Reaktionen, der opstår, er:
SO2 (G) + H2O (L) ⇌ H2SO3 (aq)
Denne reaktion er reversibel, hvilket betyder, at den svovlsyre kan nedbrydes tilbage i svovldioxid og vand.
Bemærk: Denne reaktion er også ansvarlig for dannelsen af surt regn. Når svovldioxid frigøres i atmosfæren, kan det opløses i regnvand og danne svovlsyre, som derefter kan falde til jorden som surt regn.
Sidste artikelLækker legeringshjul luft i under nul temps?
Næste artikelHvad er indholdet af et reaktionsdokument?
 Varme artikler
Varme artikler
-
 Modificeret svamp kunne genvinde olieforurenende stoffer fra arktiske farvandeKredit:Unsplash/CC0 Public Domain Forskere har udviklet en bæredygtig og økonomisk måde at genvinde olie fra ultrakoldt industrielt spildevand og olieudslip. Forskere fra Imperial College London
Modificeret svamp kunne genvinde olieforurenende stoffer fra arktiske farvandeKredit:Unsplash/CC0 Public Domain Forskere har udviklet en bæredygtig og økonomisk måde at genvinde olie fra ultrakoldt industrielt spildevand og olieudslip. Forskere fra Imperial College London -
 COVID-åndedrætstest-kan det være det næste? Forskning siger jaFra venstre:University of Canterbury forskere postdoktor Dr. Fiona Given og lektor Deborah Crittenden ved Biomolecular Interaction Center. Kredit:University of Canterbury Enhver, der har oplevet e
COVID-åndedrætstest-kan det være det næste? Forskning siger jaFra venstre:University of Canterbury forskere postdoktor Dr. Fiona Given og lektor Deborah Crittenden ved Biomolecular Interaction Center. Kredit:University of Canterbury Enhver, der har oplevet e -
 Papir eller plastik? Stiv vandtæt belægning til papir har til formål at reducere vores afhængigh…En klassisk origami-kran lavet af papir og belagt med Choetsu (venstre) og ubestrøget (højre). Når den er nedsænket i vand, holder den belagte papirkran sin form, mens den ubestrøede hurtigt mættes me
Papir eller plastik? Stiv vandtæt belægning til papir har til formål at reducere vores afhængigh…En klassisk origami-kran lavet af papir og belagt med Choetsu (venstre) og ubestrøget (højre). Når den er nedsænket i vand, holder den belagte papirkran sin form, mens den ubestrøede hurtigt mættes me -
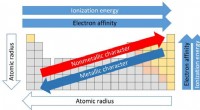 Forståelse af det periodiske system gennem linsen af de flygtige gruppe I metallerTendenser i det periodiske system. Kredit:Sandbh/Wikipedia, CC BY-SA Nyheden brød ud, at en jernbanevogn, fyldt med rent natrium, var lige afsporet og spildte dens indhold. En tv-reporter ringede
Forståelse af det periodiske system gennem linsen af de flygtige gruppe I metallerTendenser i det periodiske system. Kredit:Sandbh/Wikipedia, CC BY-SA Nyheden brød ud, at en jernbanevogn, fyldt med rent natrium, var lige afsporet og spildte dens indhold. En tv-reporter ringede
- NASA klimaforsker og astronaut Sellers dør i en alder af 61
- Sådan laver du en 7. klasse Solar Oven Shoebox Project
- Hvis morens DNA er en og barnepos, hvad far?
- Oliespildskatastrofer i de sidste 50 år
- Mikrobiel økologi giver ny indsigt i fremtidens bevarelse af skibbrud
- Er overfiskning afsluttet? Top amerikansk videnskabsmand siger ja


