Hvorfor vand anvendt i methylethanoathydrolyse?
* vand er en reaktant: Hydrolyse er i det væsentlige bagsiden af esterificering. I denne reaktion reagerer esteren (methylethanoat) med vand for at danne den tilsvarende carboxylsyre (ethansyre) og alkohol (methanol).
* Vand fungerer som et opløsningsmiddel: Vand fungerer som et opløsningsmiddel for både reaktanter og produkter, så de kan interagere lettere. Dette hjælper reaktionen med at fortsætte med en hurtigere hastighed.
Her er en mere detaljeret forklaring:
Methylethanoat (CH3COOCH3) er en ester, dannet af reaktionen af ethansyre (CH3COOH) og methanol (CH3OH). Hydrolyse -reaktionen bryder denne esterbinding ved hjælp af vand som reaktant:
CH3COOCH3 + H2O → CH3COOH + CH3OH
* mekanisme: Vandmolekylet fungerer som en nukleofil og angriber carbonylcarbonet i esteren. Dette fører til brud på esterbindingen og dannelsen af et mellemprodukt. Dette mellemprodukt reagerer derefter med et andet vandmolekyle for at danne de endelige produkter, ethansyre og methanol.
Hvorfor ikke andre opløsningsmidler?
Mens andre opløsningsmidler kan bruges, er vand især egnet, fordi:
* Det er et polært opløsningsmiddel: Dette muliggør bedre solvation af de polære reaktanter og produkter.
* Det er relativt billigt og let tilgængeligt.
I resuméet Vand er afgørende for methylethanoathydrolyse, fordi det fungerer som både reaktant og et opløsningsmiddel, der letter reaktionen og tillader det at fortsætte glat.
 Varme artikler
Varme artikler
-
 Anvendelse af beregningskemi til at simulere realistiske kemiske processerKredit:University of California - San Diego Videnskabens vand er mudret i disse dage - især ved University of California San Diego, hvor alt, der adskiller en kemiker fra en fysiker, i nogle tilfæ
Anvendelse af beregningskemi til at simulere realistiske kemiske processerKredit:University of California - San Diego Videnskabens vand er mudret i disse dage - især ved University of California San Diego, hvor alt, der adskiller en kemiker fra en fysiker, i nogle tilfæ -
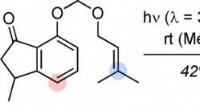 Total syntese af sesquiterpen agarozizanol BKredit:Wiley Med udgangspunkt i tilgængelige kemikalier, et tysk team af forskere gennemførte med succes den totale syntese af agarozizanol B, et interessant naturligt stof, der findes i agartræ.
Total syntese af sesquiterpen agarozizanol BKredit:Wiley Med udgangspunkt i tilgængelige kemikalier, et tysk team af forskere gennemførte med succes den totale syntese af agarozizanol B, et interessant naturligt stof, der findes i agartræ. -
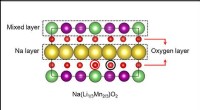 Nyt materiale kan hjælpe med at reducere batteriomkostningerne til elbiler, mobiltelefonerForskere ved University of Texas i Dallas og Seoul National University har designet et nyt batterikatodemateriale, der muligvis giver lavere omkostninger, mere miljøvenlig mulighed for lithium-ion-bat
Nyt materiale kan hjælpe med at reducere batteriomkostningerne til elbiler, mobiltelefonerForskere ved University of Texas i Dallas og Seoul National University har designet et nyt batterikatodemateriale, der muligvis giver lavere omkostninger, mere miljøvenlig mulighed for lithium-ion-bat -
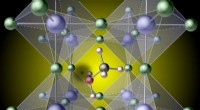 Brint i hybridperovskiter er mindre uskyldigt, end det ser udEn brinttomgang (den sorte plet til venstre for midten) skabt ved at fjerne brint fra et methylammoniummolekyle, fanger bærere i den prototypiske hybridperovskit, mehtylammonium blyiodid CH3NH3Pbl3. K
Brint i hybridperovskiter er mindre uskyldigt, end det ser udEn brinttomgang (den sorte plet til venstre for midten) skabt ved at fjerne brint fra et methylammoniummolekyle, fanger bærere i den prototypiske hybridperovskit, mehtylammonium blyiodid CH3NH3Pbl3. K
- Vores klima har ændret sig. Hvordan lærer vi at leve med ekstreme begivenheder?
- Kræftlægemidler kunne leveres i molekylære bure låst op af lys
- Undersøgelse af, hvordan mikrobiomer påvirker vores helbred
- Hvordan genomdiversiteten af store afgrøder fortæller historien om deres udvikling
- Forskere afslører ny rolle for nitrogenoxid
- Detektorforbedringer opgraderer videnskabelige muligheder for SNS- og HFIR-instrumenter


