Når halvdelen af vandet i 1 m soln sucrose koges af, hvad sker der concrose?
* Molaritet (M): Molaritet er et mål for koncentration defineret som mol af opløst stof pr. Liter opløsning.
* kogende vand: Kogende vand reducerer opløsningens volumen.
* Konstant mol: Antallet af mol saccharose forbliver det samme, fordi saccharosen ikke fjernes.
* Øget koncentration: Med færre liter opløsning, men det samme antal mol saccharose, øges molariteten (koncentrationen).
Eksempel:
Lad os sige, at du starter med 1 liter af en 1 m saccharose -løsning. Dette betyder, at du har 1 mol saccharose opløst i opløsningen.
* start: 1 mol saccharose / 1 L opløsning =1m
* efter kogning: Du koger halvdelen af vandet og efterlader 0,5 L opløsning. Molen af saccharose er stadig 1.
* Final: 1 mol sucrose / 0,5 L opløsning =2m
Koncentrationen af sucroseopløsningen er fordoblet.
Sidste artikelHvorfor vand anvendt i methylethanoathydrolyse?
Næste artikelEr formlen C6H12O6 en kolloid?
 Varme artikler
Varme artikler
-
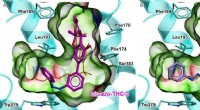 Berusende lysfølsommeTo lysfølsomme THC -derivater, og hvordan de er indlejret i cannabinoidreceptoren 1. Kredit:fra Westphal MV et al. J. Am. Chemical Soc., 2017, 139 (50), s. 18206-18212. ETH -kemikere har syntetise
Berusende lysfølsommeTo lysfølsomme THC -derivater, og hvordan de er indlejret i cannabinoidreceptoren 1. Kredit:fra Westphal MV et al. J. Am. Chemical Soc., 2017, 139 (50), s. 18206-18212. ETH -kemikere har syntetise -
 Innovativ behandling forhindrer spredning af bakterier på tværs af metaloverfladerDette billede viser en peptidfrigivelsestest, med den øgede lilla farve, der viser, at flere peptider frigives. Kredit:Purdue University Forskere ved Purdue University har udviklet en behandling t
Innovativ behandling forhindrer spredning af bakterier på tværs af metaloverfladerDette billede viser en peptidfrigivelsestest, med den øgede lilla farve, der viser, at flere peptider frigives. Kredit:Purdue University Forskere ved Purdue University har udviklet en behandling t -
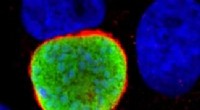 Malaria kaprer dine gener for at invadere din leverI de tidlige stadier af infektion, malariaparasitten (grøn) gemmer sig i en persons leverceller (blå), før den invaderer deres blod. Vist med rødt er et menneskeligt protein, som parasitten co-opterer
Malaria kaprer dine gener for at invadere din leverI de tidlige stadier af infektion, malariaparasitten (grøn) gemmer sig i en persons leverceller (blå), før den invaderer deres blod. Vist med rødt er et menneskeligt protein, som parasitten co-opterer -
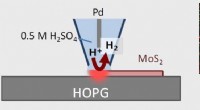 Billedbehandlingsteknik giver katalytisk 2-D materialeteknik et bedre udsynScanning elektrokemisk cellemikroskopi (SECCM) muliggør billeddannelse og kvantitativ analyse af hydrogenudviklingsreaktion (HER) katalytisk aktive steder i 1H MoS 2 monolag. Kredit:Kanazawa Univers
Billedbehandlingsteknik giver katalytisk 2-D materialeteknik et bedre udsynScanning elektrokemisk cellemikroskopi (SECCM) muliggør billeddannelse og kvantitativ analyse af hydrogenudviklingsreaktion (HER) katalytisk aktive steder i 1H MoS 2 monolag. Kredit:Kanazawa Univers
- Hvorfor små mikrober kan være en stor faktor i, hvordan klimaændringer udspiller sig
- Startup kommercialiserer MRI-enheder, der kan forbedre medicinsk diagnostik
- Hvad er nogle sande udsagn om væsker?
- Hvad kaldes det, når tågen begynder at kollapse og blive til en lille spindingsky?
- Hvor mange atomer er der i Ca(NO)2?
- Undersøgelse:På Facebook og Twitter er dit privatliv i fare – også selvom du ikke har en konto


