Hvorfor er det vigtigt at have ioner i en løsning til at udføre elektricitet?
* Elektricitet er strømmen af ladning: En elektrisk strøm er i det væsentlige bevægelse af ladede partikler.
* ioner er ladede partikler: Ioner er atomer eller molekyler, der har opnået eller mistet elektroner, hvilket resulterer i en nettopositive eller negative ladning.
* fri bevægelighed er nøglen: For at elektricitet skal flyde gennem en løsning, skal de ladede partikler være i stand til at bevæge sig frit.
* ioner i opløsning: Når ioner opløses i en opløsning, er de omgivet af opløsningsmiddelmolekyler (som vand) og kan bevæge sig uafhængigt. Dette giver dem mulighed for at bære den elektriske ladning.
Her er et eksempel:
Forestil dig en opløsning af bordsalt (NaCl) i vand. Når salt opløses, bryder det ned i natriumioner (Na+) og chloridioner (Cl-). Disse ioner er nu frie til at bevæge sig i løsningen. Hvis du påfører en spænding på tværs af opløsningen, bevæger de positive natriumioner bevæger sig mod den negative elektrode, og de negative chloridioner bevæger sig mod den positive elektrode, hvilket skaber en elektrisk strøm.
I modsætning hertil udfører rent vand ikke elektricitet godt, fordi det har meget få frie ioner. Tilsætning af opløste salte eller syrer, der frigiver ioner i opløsningen, øger dens ledningsevne markant.
Sammenfattende er tilstedeværelsen af ioner i en løsning vigtig for elektrisk ledningsevne, fordi de fungerer som mobilafgiftsselskaber, hvilket giver mulighed for strøm af elektrisk strøm.
Sidste artikelHvordan opbevares kalium i laboratoriet?
Næste artikelHvad er sædvanlige enheder af opløselighed på kurver?
 Varme artikler
Varme artikler
-
 Vandoverfladen er et fantastisk sted for kemiske reaktionerKredit:Pixabay/CC0 Public Domain Ved at bruge en avanceret teknik, forskere fra RIKEN-klyngen for banebrydende forskning har påvist, at en kemisk reaktion drevet af lys finder sted ti tusinde gang
Vandoverfladen er et fantastisk sted for kemiske reaktionerKredit:Pixabay/CC0 Public Domain Ved at bruge en avanceret teknik, forskere fra RIKEN-klyngen for banebrydende forskning har påvist, at en kemisk reaktion drevet af lys finder sted ti tusinde gang -
 Forskere udvikler nanoporøs super-multi-element katalysatorKredit:Japan Science and Technology Agency (JST) En fælles forskergruppe ledet af forskningsassistent Cai ZeXing og professor Takeshi Fujita ved School of Environmental Science and Engineering, Ko
Forskere udvikler nanoporøs super-multi-element katalysatorKredit:Japan Science and Technology Agency (JST) En fælles forskergruppe ledet af forskningsassistent Cai ZeXing og professor Takeshi Fujita ved School of Environmental Science and Engineering, Ko -
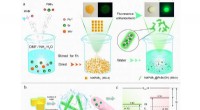 Blyhalogenid perovskiter med forbedret luminescens og stabiliteta) Skematisk diagram af synteseprocessen for MAPbBr3@PbBr(OH). b) Skematisk illustration af morfologiudviklingen af den fremstillede MAPbBr3-perovskit. c) Energiniveaudiagram af PbBr(OH) og indre QD
Blyhalogenid perovskiter med forbedret luminescens og stabiliteta) Skematisk diagram af synteseprocessen for MAPbBr3@PbBr(OH). b) Skematisk illustration af morfologiudviklingen af den fremstillede MAPbBr3-perovskit. c) Energiniveaudiagram af PbBr(OH) og indre QD -
 Selvhelbredende materiale kan bygge sig selv af kulstof i luftenDiagrammer illustrerer det nye materiales selvhelbredende egenskaber. Øverst, der dannes en revne i materialet, som er sammensat af en hydrogel (mørkegrøn) med planteafledte kloroplaster (lysegrøn) in
Selvhelbredende materiale kan bygge sig selv af kulstof i luftenDiagrammer illustrerer det nye materiales selvhelbredende egenskaber. Øverst, der dannes en revne i materialet, som er sammensat af en hydrogel (mørkegrøn) med planteafledte kloroplaster (lysegrøn) in
- Undersøgelse afslører proteiners nøglerolle i at hjælpe cilium med at transmittere signaler til …
- At bruge misundelse som et marketingværktøj kan give bagslag
- Vær på vagt over for svindlere, nogle tips
- Hvad sydafrikanske kvinder fortalte os om at være hovedforsørgeren
- Find galakser med aktive kerner
- Dyreintelligens og AI:Konkurrence er i vingerne


