Hvilket salt giver flammer grøn farve?
Her er hvorfor:
* flammeforsøg: Flammetest er en almindelig måde at identificere visse elementer på. Når et metalsalt opvarmes i en flamme, absorberer elektronerne i metalionerne energi og springer til højere energiniveau. Når de falder tilbage til deres jordtilstand, frigiver de denne energi som lys, som vi ser som en farvet flamme.
* kobber: Kobberioner (cu²⁺) udsender grønt lys, når den er ophidset i en flamme.
* kobber (ii) chlorid: Kobber (II) Chlorid er et almindeligt og opløseligt salt, der let producerer kobberioner i opløsning.
Bemærk: Andre kobbersalte, som kobber (II) sulfat (cuso₄), kan også producere en grøn flamme, men kobber (II) chlorid er ofte det mest let tilgængelige og bruges til dette formål.
Sidste artikelHvem finder ud af, at atomer med samme atomnummer, men forskellig masse?
Næste artikelHvor mange elektroner har k plus?
 Varme artikler
Varme artikler
-
 Mikro-/nano-arkitekturer i MOF-membran fremskynder olie-vandseparation(en, b) SEM-billeder og (c) af AFM-billede ZIF-8-belagt mesh-membran; (d) Fotografiet af flere oliedråber på ZIF-8-belagt mesh-membran. Kredit:© Science China Press Hyppige olieudslip under olietr
Mikro-/nano-arkitekturer i MOF-membran fremskynder olie-vandseparation(en, b) SEM-billeder og (c) af AFM-billede ZIF-8-belagt mesh-membran; (d) Fotografiet af flere oliedråber på ZIF-8-belagt mesh-membran. Kredit:© Science China Press Hyppige olieudslip under olietr -
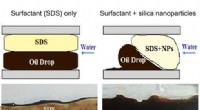 Nye materialer med vigtige anvendelser i forbedret oliegenvindingForskelle i bevægelsen af olie gennem mikrokanalerne ved tilsætning af overfladeaktivt stof i nærvær af silicananopartikler sammenlignet med det overfladeaktive middel alene, hvilket viser, hvordan
Nye materialer med vigtige anvendelser i forbedret oliegenvindingForskelle i bevægelsen af olie gennem mikrokanalerne ved tilsætning af overfladeaktivt stof i nærvær af silicananopartikler sammenlignet med det overfladeaktive middel alene, hvilket viser, hvordan -
 Karakterisering af proteinkondensaters tidsafhængige materialeegenskaberProteindråber udviser aldersafhængige materialeegenskaber. Kredit: Videnskab (2020). DOI:10.1126/science.aaw4951 Et team af forskere tilknyttet flere institutioner i Tyskland og Østrig har udvikl
Karakterisering af proteinkondensaters tidsafhængige materialeegenskaberProteindråber udviser aldersafhængige materialeegenskaber. Kredit: Videnskab (2020). DOI:10.1126/science.aaw4951 Et team af forskere tilknyttet flere institutioner i Tyskland og Østrig har udvikl -
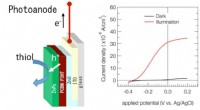 Miljøvenlige elektrokemiske katalysatorer, der bruger solceller til at høste energi fra solenStrukturen af den foreslåede enhed, viser, hvordan de genererede huller (h+) bruges til at lette thioloxidation. Den målte strøm stiger dramatisk under belysning og anvendelse af et lille potentiale
Miljøvenlige elektrokemiske katalysatorer, der bruger solceller til at høste energi fra solenStrukturen af den foreslåede enhed, viser, hvordan de genererede huller (h+) bruges til at lette thioloxidation. Den målte strøm stiger dramatisk under belysning og anvendelse af et lille potentiale
- Et skridt nærmere biotekniske erstatninger for skibe og kanaler
- Hvilken cellulær struktur var synligt almindelig for alle typer muskelceller?
- Er lithium en kation eller anion?
- En metode til fremstilling af 3D-Bose-Einstein-kondensater ved hjælp af laserkøling
- Team afslører regler for fremstilling af ribben
- Stadig varmere europæiske somre skader sundheden, siger rapporten


