Hvad ændrer gasopløselighed?
1. Temperatur:
* Inverse forhold: Når temperaturen stiger, falder gasopløselighed. Tænk på en kulsyreholdig drik, der går fladt, når den varmer op. Gassen (CO2) slipper lettere ud ved højere temperaturer.
2. Tryk:
* Direkte forhold: Når trykket øges, øges gasopløseligheden. Dette er Henrys lov, der siger, at opløseligheden af en gas er direkte proportional med det delvise tryk på gassen over væsken. Dette er grunden til, at SCUBA -dykkere er nødt til at være forsigtige med dekomprimeringssyge, da kvælstofgas opløses lettere i deres blod ved højere tryk under vandet.
3. Gasens art:
* forskellige gasser, forskellige opløseligheder: Nogle gasser er mere opløselige end andre. For eksempel er kuldioxid (CO2) meget mere opløseligt i vand end nitrogen (N2).
4. Opløsningsmidlets art:
* som opløser som: Polære opløsningsmidler (som vand) har en tendens til at opløse polære gasser bedre, mens ikke -polære opløsningsmidler (som olie) opløser ikke -polære gasser lettere. For eksempel opløses ilt (O2) bedre i vand end i olie.
5. Tilstedeværelse af andre opløste stoffer:
* Salting ud: Tilsætning af salte til en opløsning kan reducere opløseligheden af gasser. Dette skyldes, at saltioner interagerer med vandmolekylerne, hvilket gør det mindre sandsynligt, at gasmolekyler opløses.
6. Omrøring eller agitation:
* hurtigere opløsning: Omrøring eller agitering af en opløsning kan øge den hastighed, hvormed en gas opløses, men den øger ikke nødvendigvis den samlede opløselighed.
Kortfattet:
Gasopløselighed er et komplekst fænomen påvirket af en kombination af faktorer. At forstå disse faktorer er afgørende inden for mange områder, såsom kemi, biologi og teknik, hvor gasopløselighed spiller en betydelig rolle i forskellige processer.
Sidste artikelHvorfor er polyethylen et højt smeltende fast stof?
Næste artikelBrug af kemi i plastindustrier?
 Varme artikler
Varme artikler
-
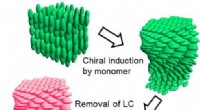 Metode til at skabe optisk aktive polymerer ved hjælp af en spiralformet flydende krystalskabelonGrafisk abstrakt. Kredit:Molekylære krystaller og flydende krystaller (2022). DOI:10.1080/15421406.2022.2073421 En videnskabsmand fra Fakultetet for Rene og Anvendte Videnskaber ved University of T
Metode til at skabe optisk aktive polymerer ved hjælp af en spiralformet flydende krystalskabelonGrafisk abstrakt. Kredit:Molekylære krystaller og flydende krystaller (2022). DOI:10.1080/15421406.2022.2073421 En videnskabsmand fra Fakultetet for Rene og Anvendte Videnskaber ved University of T -
 Hydrogelbaserede elektroder til hjerneimplantater udvikletPrøve af hydrogel udviklet. Kredit:Kizkitza Gonzalez / UPV / EHU Hydrogeler er fysiske og kemiske polymernetværk, der er i stand til at tilbageholde store mængder væske under vandige forhold uden
Hydrogelbaserede elektroder til hjerneimplantater udvikletPrøve af hydrogel udviklet. Kredit:Kizkitza Gonzalez / UPV / EHU Hydrogeler er fysiske og kemiske polymernetværk, der er i stand til at tilbageholde store mængder væske under vandige forhold uden -
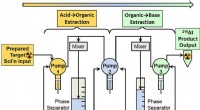 Modulært fluidsystem udviklet til at levere radioisotop, der anvendes i målrettet alfa-terapiSkematisk af opløsningsmiddelekstraktionsmodul til astatin-211 (211At) isolering fra opløst bismuth cyclotron target. Processen starter i venstre side og fortsætter til højre. Kredit:Matthew OHara, Pa
Modulært fluidsystem udviklet til at levere radioisotop, der anvendes i målrettet alfa-terapiSkematisk af opløsningsmiddelekstraktionsmodul til astatin-211 (211At) isolering fra opløst bismuth cyclotron target. Processen starter i venstre side og fortsætter til højre. Kredit:Matthew OHara, Pa -
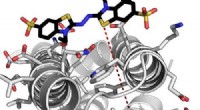 Kunstige enzymfunktioner samt naturlig versionBeregningsmodel for et yderst effektivt de novo -enzym, der interagerer med et af dets substrater. Den røde stiplede linje angiver elektrontunnelafstanden mellem det proteinbundne hæmmolekyle og det b
Kunstige enzymfunktioner samt naturlig versionBeregningsmodel for et yderst effektivt de novo -enzym, der interagerer med et af dets substrater. Den røde stiplede linje angiver elektrontunnelafstanden mellem det proteinbundne hæmmolekyle og det b
- Satellitkort over menneskets pres på land giver indsigt i bæredygtig udvikling
- Hvordan kan geologer udlede af sedimentære bjergarter, hvordan fortidens overfladeforhold var?
- Forskning viser, at præferencen for mandlige børn er faldende i Bangladesh
- Kan du lave et WiFi -netværk ud af en bus?
- Hvorfor er det så koldt i Australien lige nu? Og hvor længe vil det vare? En klimaforsker forklare…
- Fremstilling af batterier fra den tomme luft


