Hvorfor er metaller gode ledere af elektricitet giver mindst 4 grunde?
1. Gratis elektroner: Metaller har en unik struktur, hvor deres yderste elektroner er løst bundet til atomerne. Disse elektroner er i det væsentlige frie til at bevæge sig gennem det metalliske gitter. Dette "hav" af frie elektroner er det, der gør metaller fremragende ledere.
2. svagt bundne elektroner: Den elektrostatiske tiltrækning mellem metalatomerne og deres yderste elektroner er relativt svag. Denne svage attraktion giver elektroner mulighed for let at løsrive sig fra atomer og blive mobile.
3. Bestilt struktur: Den regelmæssige, krystallinske struktur af metaller giver elektroner mulighed for at bevæge sig frit uden betydelige kollisioner. Dette bestilte arrangement hjælper med at lette ladningsstrømmen.
4. Høj densitet af elektroner: Metaller har generelt en høj densitet af atomer pakket sammen. Denne høje densitet betyder, at der er et stort antal frie elektroner til rådighed til at transportere elektrisk strøm.
Kortfattet: Metaller er gode ledere af elektricitet, fordi de har en rigelig forsyning med løst bundet, frie elektroner, der let kan bevæge sig gennem deres struktur. Denne frie bevægelse af elektroner giver mulighed for effektiv ladningstransport.
 Varme artikler
Varme artikler
-
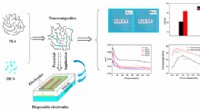 Nedbrydelige elektroniske komponenter fremstillet af majsstivelseKredit:American Chemical Society Efterhånden som forbrugerne opgraderer deres gadgets i et stigende tempo, mængden af elektronisk affald, vi genererer, fortsætter med at stige. For at hjælpe med
Nedbrydelige elektroniske komponenter fremstillet af majsstivelseKredit:American Chemical Society Efterhånden som forbrugerne opgraderer deres gadgets i et stigende tempo, mængden af elektronisk affald, vi genererer, fortsætter med at stige. For at hjælpe med -
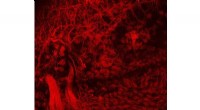 Ænder giver forskere en unik mulighed for at studere menneskelig berøringEt lysarkmikroskopbillede af embryonal andenæshud farvet med Tuj1-antistoffer til at mærke sensoriske neuroner. Kredit:Slav Bagriantsev Hvis den går som en and (eller en gås eller en svane), den k
Ænder giver forskere en unik mulighed for at studere menneskelig berøringEt lysarkmikroskopbillede af embryonal andenæshud farvet med Tuj1-antistoffer til at mærke sensoriske neuroner. Kredit:Slav Bagriantsev Hvis den går som en and (eller en gås eller en svane), den k -
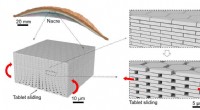 Ny type glas inspireret af naturen er mere modstandsdygtig over for stødMikroarkitekturen af Nacre og tablet, der glider i Nacre. Kredit:Z. Yin, F. Hannard, F. Barthelat Ved at bruge den iriserende perlemor, der ofte findes foring af muslingeskaller, forskere har ko
Ny type glas inspireret af naturen er mere modstandsdygtig over for stødMikroarkitekturen af Nacre og tablet, der glider i Nacre. Kredit:Z. Yin, F. Hannard, F. Barthelat Ved at bruge den iriserende perlemor, der ofte findes foring af muslingeskaller, forskere har ko -
 Hvordan varme (og ikke så varme) forbindelser i chilipeber ændrer sig under modningKredit:CC0 Public Domain Enhver, der har smagt en varm chilipeber, har mærket forbrændingen af capsaicinoider, forbindelser, der giver peberfrugter deres krydderi, samt mulige sundhedsmæssige fo
Hvordan varme (og ikke så varme) forbindelser i chilipeber ændrer sig under modningKredit:CC0 Public Domain Enhver, der har smagt en varm chilipeber, har mærket forbrændingen af capsaicinoider, forbindelser, der giver peberfrugter deres krydderi, samt mulige sundhedsmæssige fo
- Hvad er standardreduktionspotentialet E for halvreaktion Mg2 (aq) 2e mg (s)?
- Nyt paradigme inden for atmosfærisk gassensing og molekylær identifikation
- Hvor er femogtyve procent af nikkelmalmen udvindet?
- Med St. Amands matrix, byplanlæggere kan identificere udsatte arkæologiske steder
- Afstande af planeterne fra solen i lysårene
- Xerox CEO forbliver, da Icahn-aftalens deadline udløber


