Forklar, hvorfor damptrykket reduceres i en opløsning med ikke -flygtig opløst stof?
Forståelse af damptryk
* rent opløsningsmiddel: I en ren væske undslipper molekyler konstant fra overfladen og går ind i dampfasen (fordampning). Det tryk, der udøves af disse dampmolekyler, kaldes damptrykket.
* ligevægt: Ved en given temperatur nås en dynamisk ligevægt, hvor fordampningshastigheden svarer til kondensationshastigheden.
Effekten af et ikke -flygtigt opløst stof
* ikke -flygtig: Et ikke -flygtigt opløst stof er en, der ikke let fordampes. Eksempler inkluderer salte som NaCl eller sukker.
* reduceret overfladeareal: Når et ikke -flygtigt opløst stof tilsættes til et opløsningsmiddel, reducerer det effektivt det tilgængelige overfladeareal til opløsningsmiddelmolekyler for at flygte ind i dampfasen. Tænk på det som at have en overfyldt overflade - mindre plads til opløsningsmiddelmolekyler til at bryde fri.
* Intermolekylære interaktioner: Solute -partiklerne kan også danne intermolekylære interaktioner med opløsningsmiddeltemolekylerne, hvilket yderligere hindrer deres flugt. Disse interaktioner kan være stærkere end opløsningsmiddelopløsningsmidlets interaktioner, hvilket gør det vanskeligere for opløsningsmiddelmolekyler at bryde fri og komme ind i dampfasen.
Raoults lov:Kvantificering af effekten
Raoults lov beskriver forholdet mellem damptryk og tilstedeværelsen af et ikke -flygtigt opløst stof:
* p løsning =X opløsningsmiddel * P opløsningsmiddel
* P løsning :Damptrykket af opløsningen
* X opløsningsmiddel :Molfraktion af opløsningsmidlet (andelen af opløsningsmiddelmolekyler i opløsningen)
* P opløsningsmiddel :Damptrykket af det rene opløsningsmiddel
Denne ligning viser, at opløsningens damptryk er direkte proportionalt med molfraktionen af opløsningsmidlet. Da molfraktionen af opløsningsmidlet falder med tilsætningen af et opløst stof, falder damptrykket af opløsningen også.
Kortfattet
Tilstedeværelsen af et ikke -flygtigt opløst stof reducerer damptrykket af en opløsning, fordi den:
1. reducerer overfladearealet Tilgængelig til opløsningsmiddelfordampning.
2. øger intermolekylære interaktioner , hvilket gør det sværere for opløsningsmiddelmolekyler at flygte.
Denne reduktion i damptryk er direkte relateret til molfraktionen af opløsningsmidlet som beskrevet af Raoults lov.
Sidste artikelEr en cykel, der ruster i regnskiftet regn?
Næste artikelHvad er atommassen for dette atom 19p og 20n?
 Varme artikler
Varme artikler
-
 Sådan forbliver muslinger isfri i en iskold verdenPå grund af en regelmæssig overfladestruktur på muslingen Adamussium colbecki klæber isen kun meget svagt til den og kan let skylles væk af strøm. Kredit:Max Planck Institute for Polymer Research A
Sådan forbliver muslinger isfri i en iskold verdenPå grund af en regelmæssig overfladestruktur på muslingen Adamussium colbecki klæber isen kun meget svagt til den og kan let skylles væk af strøm. Kredit:Max Planck Institute for Polymer Research A -
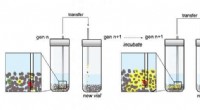 Livlig kemi skabt i laboratoriesøgning efter måder at studere livets oprindelse påForskerne udsatte deres kemiske supper for en form for selektion ved at tage en lille mængde materiale fra et hætteglas og placere det i et nyt hætteglas med frisk pyrit og kemikalier. Efter flere gen
Livlig kemi skabt i laboratoriesøgning efter måder at studere livets oprindelse påForskerne udsatte deres kemiske supper for en form for selektion ved at tage en lille mængde materiale fra et hætteglas og placere det i et nyt hætteglas med frisk pyrit og kemikalier. Efter flere gen -
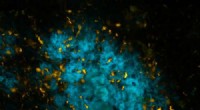 Skinnende molekyler skelner mellem proteiner i hjernenHjernevæv med Alzheimers patologi, farvet med et af de nye tau-specifikke molekyler (orange) og et af de molekyler, der tidligere er udviklet af gruppen ved LiU (blå). Billedet er taget i et fluoresce
Skinnende molekyler skelner mellem proteiner i hjernenHjernevæv med Alzheimers patologi, farvet med et af de nye tau-specifikke molekyler (orange) og et af de molekyler, der tidligere er udviklet af gruppen ved LiU (blå). Billedet er taget i et fluoresce -
 Gennembrud for origami-diagnostik er til gavn for landmænd i udviklingslandeneKredit: ACS sensorer (2018). DOI:10.1021/acssensors.7b00825 Ark foldet papir, trykt med voks, kunne være nøglen til at udvikle meget billig diagnostik for at forbedre sundheden for husdyr i lav-
Gennembrud for origami-diagnostik er til gavn for landmænd i udviklingslandeneKredit: ACS sensorer (2018). DOI:10.1021/acssensors.7b00825 Ark foldet papir, trykt med voks, kunne være nøglen til at udvikle meget billig diagnostik for at forbedre sundheden for husdyr i lav-
- Hvor mange yderligere elektroner har et hydrogenatom behov for at afslutte sine yderste energiniveau…
- Er nul grader Kelvin det samme som Fahrenheit?
- Hvorfor vi ikke kan stole på, at virksomheder kan redde os fra klimaændringer
- Underjordisk nanometri:Undersøgelse af skjulte materialer via atomkraftmikroskopi
- Hvorfor er himlen blå?
- Hvad er nogle ting lavet af platin?


