Skinnende molekyler skelner mellem proteiner i hjernen
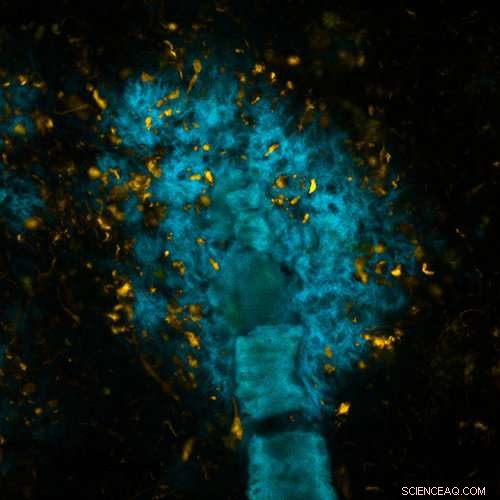
Hjernevæv med Alzheimers patologi, farvet med et af de nye tau-specifikke molekyler (orange) og et af de molekyler, der tidligere er udviklet af gruppen ved LiU (blå). Billedet er taget i et fluorescensmikroskop. Kredit:Peter R Nilsson
Små skinnende molekyler udviklet af forskere ved Linköpings Universitet i Sverige kan designes til at skelne mellem plak af forskellige proteiner i hjernen. De kan bane vejen for bedre diagnosticering af neurodegenerative sygdomme, såsom Alzheimers sygdom, hvor plaque dannes fra amyloid beta- eller tau-proteinerne.
Forskere ved Linköpings Universitet, LiU, har opdaget, at små ændringer i strukturen af kendte spormolekyler kan sætte dem i stand til at genkende enten amyloid beta eller tau. Disse små molekyler, som tidligere er udviklet af forskerne, binder til et specifikt målprotein. Når molekylerne er belyst, de udsender et signal i form af lys ved en anden bølgelængde.
"Dette åbner muligheden for at udvikle mere avancerede diagnostiske værktøjer til sygdomme, hvor amyloid beta og tau er involveret, siger Peter Nilsson, professor ved Institut for Fysik, Kemi og biologi. Han har ledet undersøgelsen, som nu er blevet præsenteret i det videnskabelige tidsskrift Kemi – Et europæisk tidsskrift .
Ved flere sygdomme i hjernen, lange proteinfibre, og til sidst bliver sammenfiltret for at danne tætte kroppe kendt som "plak" eller "aggregater". Alzheimers sygdom, som forårsager demens, er et velkendt eksempel, hvor pladen normalt består af defekte varianter af to proteiner:amyloid beta og tau. Men aflejringer af tau-proteinet i hjernen ses også i en gruppe af mindre almindelige tilstande kendt som "tauopatier".
I de seneste år, flere tilfælde af hjerneskade hos relativt unge mennesker med en professionel idrætskarriere er der blevet skrevet meget om. Kronisk traumatisk encefalopati (CTE) kan forekomme hos personer, der har fået slag i hovedet ved gentagne lejligheder, som kan forekomme i kontaktsportsgrene såsom boksning, ishockey og amerikansk fodbold. En anden risikogruppe er professionelle soldater. Den eneste måde, der i øjeblikket er tilgængelig for at nå en fast diagnose, er under en obduktion. Dermed, der er et presserende behov for diagnostiske værktøjer, der kan bruges til at undersøge levende mennesker, og det kan skelne mellem aflejringer af amyloid beta og tau i hjernen.
Det, der gør disse molekyler unikke, er, at de har fleksible rygrad og tilpasser sig strukturen af det protein, som de er bundet til. Når molekylet ændrer sin konfiguration, farven på det lys, den udsender, ændres. Forskerne startede med et sporstofmolekyle, der kun binder sig til og genkender aggregater af amyloid beta. De tilpassede dette molekyle til at blive mere lig molekyler, der var blevet udviklet af andre forskergrupper, og som binder sig til tau. De lavede to varianter, og det viste sig, at et af molekylerne binder meget tæt og udelukkende til tau, mens den anden variant var helt uegnet.
"Vi ser, at ekstremt små ændringer, bare flytte et par atomer, kan få sporstofmolekylet til at binde sig fortrinsvis til en anden type aggregat. Det betyder, at vi kan skræddersy molekyler til at genkende forskellige aggregater, baseret på hvilket protein der er til stede, siger Peter Nilsson.
Forskerne planlægger nu at videreudvikle sporstofmolekylerne ved at mærke dem med radioisotoper, bruges under positronemissionstomografi (PET). En stor fordel ved PET-undersøgelser er, at de kan udføres på levende mennesker.
"Hvis vi kan udvikle mere avancerede diagnostiske værktøjer, der kan skelne mellem amyloid beta og tau, det ville være muligt at bestemme, hvilket proteinaggregat der dannes først, og hvordan aggregaterne interagerer. Det vil også være muligt at undersøge, om forskellige behandlingsformer er effektive mod den ene type tilslag uden at påvirke den anden, siger Peter Nilsson.
Sidste artikelDykker ned i atomområdet
Næste artikelEn ny måde at syntetisere antioxidante stoffer på
 Varme artikler
Varme artikler
-
 Revolutionær proces kunne signalere en ny æra for gensynteseKunstnerens indtryk af klik-DNA processen. Kredit:Karl Harrison Et team af forskere ledet af University of Southampton har demonstreret en banebrydende ny metode til gensyntese - et vigtigt forskn
Revolutionær proces kunne signalere en ny æra for gensynteseKunstnerens indtryk af klik-DNA processen. Kredit:Karl Harrison Et team af forskere ledet af University of Southampton har demonstreret en banebrydende ny metode til gensyntese - et vigtigt forskn -
 Nanopartikler i lithium-svovlbatterier opdaget med neutroneksperimentoperandocellen er udviklet hos HZB og gør det muligt at analysere processer inde i batteriet under opladningscyklusser med neutroner. Kredit:S. Risse/HZB Lithium-svovl-batterier betragtes som en a
Nanopartikler i lithium-svovlbatterier opdaget med neutroneksperimentoperandocellen er udviklet hos HZB og gør det muligt at analysere processer inde i batteriet under opladningscyklusser med neutroner. Kredit:S. Risse/HZB Lithium-svovl-batterier betragtes som en a -
 Kan bionedbrydelige polymerer leve op til hypen?Kredit:Pixabay/CC0 Public Domain Efterhånden som både forbrugere og virksomheder bliver mere miljøbevidste, den kemiske industri arbejder på at finde løsninger på plastikaffaldskrisen. En idé er a
Kan bionedbrydelige polymerer leve op til hypen?Kredit:Pixabay/CC0 Public Domain Efterhånden som både forbrugere og virksomheder bliver mere miljøbevidste, den kemiske industri arbejder på at finde løsninger på plastikaffaldskrisen. En idé er a -
 Ny indsigt i modning af miRNA'erForfatterne var i stand til at vise nøjagtigt, hvordan et specifikt RNA-bindende protein (blåt) genkender pri-miR-18a (pink) og ændrer dets struktur på en sådan måde, at det udvikler sig til modent mi
Ny indsigt i modning af miRNA'erForfatterne var i stand til at vise nøjagtigt, hvordan et specifikt RNA-bindende protein (blåt) genkender pri-miR-18a (pink) og ændrer dets struktur på en sådan måde, at det udvikler sig til modent mi
- NASA InSight -mission til Mars ankommer til lanceringsstedet
- En solcelledrevet asteroideplanteskole i kredsløb om Mars
- Er de konservative mere skeptiske over for klimaændringer? Det kommer an på
- Bioprocesingeniører genvinder glucosinolat fra oliefrømel
- Sådan Lær Alfabetisk & Decimal Antal Filing Systems
- Hvordan arbejdsgivere kan mildne slaget ved orlov og fyringer


