Hvor mange mol ioner frigives, når 42,1 g CUSO4IS opløstes i vand?
1. Beregn den molære masse af cuso₄:
* CU:63,55 g/mol
* S:32,06 g/mol
* O (4 atomer):16,00 g/mol x 4 =64,00 g/mol
* Total molær masse af cuso₄ =63,55 + 32,06 + 64,00 =159,61 g/mol
2. Beregn molen på cuso₄:
* Mol =masse / molær masse
* Mol cuso₄ =42,1 g / 159,61 g / mol =0,264 mol
3. Bestem de producerede ioner:
* Når cuso₄ opløses i vand, adskiller den sig til kobber (ii) ioner (cu²⁺) og sulfationer (so₄²⁻):
* Cuso₄ (aq) → cu²⁺ (aq) + so₄²⁻ (aq)
4. Beregn molen af ioner:
* Da en mol cuso₄ producerer en mol cu²⁺ og en mol so₄²⁻, er det samlede antal mol ioner:
* 0,264 mol cu²⁺ + 0,264 mol so₄²⁻ =0,528 mol ioner
Derfor er 42,1 g cuso₄ opløst i vand, 0,528 mol ioner.
 Varme artikler
Varme artikler
-
 Nyligt udviklet enzym fremskynder langsom organisk reaktionKredit:SUWIT NGAOKAEW, Shutterstock Alsidige katalysatorer med nye funktioner og funktioner kan revolutionere videnskabsmænds syntetiske strategier og bane vejen for kemikalier af høj værdi og en g
Nyligt udviklet enzym fremskynder langsom organisk reaktionKredit:SUWIT NGAOKAEW, Shutterstock Alsidige katalysatorer med nye funktioner og funktioner kan revolutionere videnskabsmænds syntetiske strategier og bane vejen for kemikalier af høj værdi og en g -
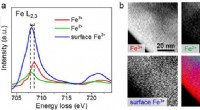 Effektiv brintomdannelse gennem solvandsopdeling ved hjælp af hæmatitmesokrystalbaserede fotoanode…Figur 1:STEM-EELS-analyse viser fordelingen af jernoxid og iltfaciliteter (Vo) i mesokrystaller. (a) EEL (Electron Energy Loss) spektre af Fe L 2, 3 ved hjælp af multivariat analyse. (b) Billede a
Effektiv brintomdannelse gennem solvandsopdeling ved hjælp af hæmatitmesokrystalbaserede fotoanode…Figur 1:STEM-EELS-analyse viser fordelingen af jernoxid og iltfaciliteter (Vo) i mesokrystaller. (a) EEL (Electron Energy Loss) spektre af Fe L 2, 3 ved hjælp af multivariat analyse. (b) Billede a -
 Ny katalysator opnår hidtil usete aktiviteterPhilip Weber og Thorsten Scherpf (til venstre) var væsentligt involveret i eksperimenterne i laboratoriet. Kredit:Ruhr-Universitaet-Bochum Forskere har udviklet en ny katalysator til syntetisering
Ny katalysator opnår hidtil usete aktiviteterPhilip Weber og Thorsten Scherpf (til venstre) var væsentligt involveret i eksperimenterne i laboratoriet. Kredit:Ruhr-Universitaet-Bochum Forskere har udviklet en ny katalysator til syntetisering -
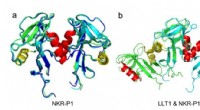 Fra atomet til naturlig dræbercelle:Historien om en uventet proteinstrukturStruktur af human NKR-P1, der viser den unikke dimeriseringsgrænseflade. Panel (a) sammenligner krystalstrukturer af NKR-P1-receptorbindende domæne-dimerer. Panel (b) viser en strukturel sammenligning
Fra atomet til naturlig dræbercelle:Historien om en uventet proteinstrukturStruktur af human NKR-P1, der viser den unikke dimeriseringsgrænseflade. Panel (a) sammenligner krystalstrukturer af NKR-P1-receptorbindende domæne-dimerer. Panel (b) viser en strukturel sammenligning
- Huawei går på 5G, mens politik spiller ud
- Google landsby i centrum af San Jose ville forbinde lokale kvarterer, virksomhedsløfter
- Uendelig-dimensionel symmetri åbner mulighed for en ny fysik-og nye partikler
- Hvordan LinkedIns søgemaskine kan afspejle en kønsbias
- Hyundai investerer 300 millioner dollars for at hjælpe Indias Ola med at kæmpe mod Uber
- Beskyttende skibsbelægninger som en undervurderet kilde til mikroplastikforurening


