Hvorfor er det usandsynligt, at calciumchloridkrystaller er fremstillet af metal?
* ionisk binding: Calciumchlorid (CACL₂) dannes gennem ionisk binding. Dette betyder, at calcium (CA), et metal, mister to elektroner for at blive en positivt ladet ion (Ca²⁺). Chlor (CL), en ikke -metal, får en elektron hver til at blive negativt ladede ioner (CL⁻). Disse modsatte ladede ioner tiltrækker hinanden stærkt og danner den ioniske sammensatte cacl₂.
* krystalstruktur: Den stærke elektrostatiske attraktion mellem ionerne fører til et stærkt organiseret, gentagende arrangement af ioner kaldet en krystalgitter. Dette er grunden til, at calciumchlorid danner krystaller.
* egenskaber ved metaller: Metaller er typisk skinnende, formbare, duktile og gode ledere af varme og elektricitet. Calciumchloridkrystaller udviser ikke disse egenskaber.
Kortfattet: Arten af ionisk binding i calciumchlorid og den resulterende krystalstruktur er grundlæggende forskellig fra egenskaberne og strukturen af metaller. Derfor er det usandsynligt, at calciumchloridkrystaller er fremstillet af metal.
Sidste artikelHvad hedder en Liguid til gas?
Næste artikelNår en kemisk reaktion finder sted?
 Varme artikler
Varme artikler
-
 Hvordan forskere bekæmper infektionsfremkaldende biofilmEn kunstnerisk skildring af en biofilm med antibiotikaresistente stavformede og sfæriske bakterier. Kredit:Kateryna Kon/Shutterstock.com De overflader, mennesker interagerer med hver dag, kan virk
Hvordan forskere bekæmper infektionsfremkaldende biofilmEn kunstnerisk skildring af en biofilm med antibiotikaresistente stavformede og sfæriske bakterier. Kredit:Kateryna Kon/Shutterstock.com De overflader, mennesker interagerer med hver dag, kan virk -
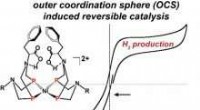 Forskere designer hurtigt, reversible bio-inspirerede katalysatorerKredit:Environmental Molecular Sciences Laboratory For at vind- og solkraft kan blive grundpillerne i vedvarende energi, den energi, de producerer med mellemrum, skal lagres og hentes effektivt. O
Forskere designer hurtigt, reversible bio-inspirerede katalysatorerKredit:Environmental Molecular Sciences Laboratory For at vind- og solkraft kan blive grundpillerne i vedvarende energi, den energi, de producerer med mellemrum, skal lagres og hentes effektivt. O -
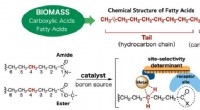 Et nyt værktøj til at skabe kemisk kompleksitet fra fedtsyrerDen nyudviklede katalysator (midterste bund) består af et metal (iridium) atom i kernen og forskellige moduler, der sikrer, at fedtsyreamid eller ester er præcist placeret på en måde, så CH -bindingen
Et nyt værktøj til at skabe kemisk kompleksitet fra fedtsyrerDen nyudviklede katalysator (midterste bund) består af et metal (iridium) atom i kernen og forskellige moduler, der sikrer, at fedtsyreamid eller ester er præcist placeret på en måde, så CH -bindingen -
 Ny teknik bringer studiet af molekylær konfiguration ind i det mikroskopiske domæneRohit Bhargava med postdoktor Kevin Yeh, der designede det brugerdefinerede infrarøde mikroskop, der blev brugt til denne undersøgelse. Dette foto er taget i februar 2020. Kredit:L. Brian Stauffer, Un
Ny teknik bringer studiet af molekylær konfiguration ind i det mikroskopiske domæneRohit Bhargava med postdoktor Kevin Yeh, der designede det brugerdefinerede infrarøde mikroskop, der blev brugt til denne undersøgelse. Dette foto er taget i februar 2020. Kredit:L. Brian Stauffer, Un
- Test viser, at disse bølger er syge, på den helt forkerte måde
- Australien har flere hjemmehørende fuglearter end næsten noget andet sted. Hvad førte til denne e…
- Fantastiske billeder fra søndagens totale måneformørkelse, da observatører spionerer
- Hvorfor kan ikke økosystemernes energi genbruges?
- Hvad er styrke?


