Har væsker de største mellemrum mellem partikler, så de kan komprimeres?
Her er en sammenbrud:
* Gasser: Partikler er langt fra hinanden og bevæger sig frit, hvilket giver mulighed for betydelig komprimering.
* væsker: Partikler er tættere sammen end gasser, men har stadig lidt plads til at bevæge sig rundt. De er mindre komprimerbare end gasser, men kan komprimeres i lille grad.
* faste stoffer: Partikler er tæt pakket og har meget lidt plads til at bevæge sig. De er meget vanskelige at komprimere.
Tænk på det sådan:Forestil dig et rum fuld af mennesker. Hvis folket står langt fra hinanden (som gasmolekyler), kan du nemt skubbe dem tættere sammen (komprimere gassen). Hvis folket er pakket skulder-til-skulder (som flydende molekyler), kan du stadig presse dem lidt, men det vil være meget sværere. Og hvis folket sidder i stole (som faste molekyler), er der næppe nogen plads til at komprimere dem.
Sidste artikelEr en glaskrukke -løsning?
Næste artikelEr partikler af en gas tæt sammen?
 Varme artikler
Varme artikler
-
 Ultra tynd, gastætte belægninger til PET-flaskerEn kapacitivt koblet plasmakilde (CCP) til generering af nanopartikler. Nanopartiklerne er indlejret i kompositlag til filtermembraner for at kontrollere selektiviteten for forskellige gasser. Kredit:
Ultra tynd, gastætte belægninger til PET-flaskerEn kapacitivt koblet plasmakilde (CCP) til generering af nanopartikler. Nanopartiklerne er indlejret i kompositlag til filtermembraner for at kontrollere selektiviteten for forskellige gasser. Kredit: -
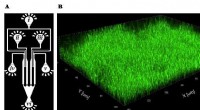 Vask genstridige biofilm væk ved hjælp af svampe rengøringsmidlerKredit:University of Tsukuba Lurer inde i rør og på overflader af medicinsk udstyr, slimede lag af bakterier, kaldet biofilm, forårsage problemer lige fra storskala produktkontaminering til potent
Vask genstridige biofilm væk ved hjælp af svampe rengøringsmidlerKredit:University of Tsukuba Lurer inde i rør og på overflader af medicinsk udstyr, slimede lag af bakterier, kaldet biofilm, forårsage problemer lige fra storskala produktkontaminering til potent -
 Forskere fremmer forståelsen af vitale enzymerDouglas Rees (til venstre) og Garnet Chan (til højre). Kredit:Caltech nitrogenaser, de enzymer, der er ansvarlige for at omdanne atmosfærisk nitrogen til de nitrogenbaserede forbindelser, der brug
Forskere fremmer forståelsen af vitale enzymerDouglas Rees (til venstre) og Garnet Chan (til højre). Kredit:Caltech nitrogenaser, de enzymer, der er ansvarlige for at omdanne atmosfærisk nitrogen til de nitrogenbaserede forbindelser, der brug -
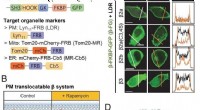 Ny undersøgelse afdækker interaktionen mellem calciumkanalerSubcellulær translokation af CaV β-underenheder ved tilsætning af rapamycin i intakt tsA-201. Kredit:Daegu Gyeongbuk Institut for Videnskab og Teknologi (DGIST) Koreanske forskere har identificere
Ny undersøgelse afdækker interaktionen mellem calciumkanalerSubcellulær translokation af CaV β-underenheder ved tilsætning af rapamycin i intakt tsA-201. Kredit:Daegu Gyeongbuk Institut for Videnskab og Teknologi (DGIST) Koreanske forskere har identificere
- Forskere hjælper migrerende laks med at overleve dødelighedens hot-spot
- Hvor meget vand i 100 fod af 6 tommer rør?
- Forskning skaber DNA-lignende molekyle for at hjælpe med at søge efter fremmed liv
- Hvor godt går for tidligt fødte børn i skolen?
- Medicinske instrumenter er steriliseret under de hotteste mulige temperaturer forklarer, hvorfor de …
- Forskelle mellem Protista & Monera


