Hvorfor er makroskopiske prøver af salte neutrale forbindelser?
* ionisk binding: Saltene dannes gennem ionisk binding. Dette betyder, at et metalatom mister en eller flere elektroner for at blive en positivt ladet ion (kation), mens et ikke -metalatom får en eller flere elektroner til at blive en negativt ladet ion (anion).
* Lige og modsatte afgifter: De resulterende kationer og anioner tiltrækkes af hinanden gennem elektrostatiske kræfter og danner en ionisk binding. Da antallet af elektroner, der er mistet af metalatomet, er lig med antallet af elektroner, der er opnået ved ikke -metalatomet, er den samlede ladning af det resulterende salt neutral.
* krystalgitterstruktur: Disse ioner arrangerer sig selv i et regelmæssigt, gentagne mønster kaldet en krystalgitter. I denne struktur fordeles de positive og negative ladninger jævnt i hele krystallen, hvilket sikrer en neutral samlet ladning.
Eksempel:
* natriumchlorid (NaCl) er et almindeligt salt. Natrium (NA) mister et elektron for at blive Na+, mens klor (CL) får en elektron til at blive Cl-. De resulterende afgifter afbalanceres, hvilket gør den sammensatte neutrale.
Undtagelser:
* Nogle salte kan udvise let surhed eller grundlæggende, når de opløses i vand. Dette skyldes interaktionen af ioner med vandmolekyler, hvilket kan føre til produktion af H+ eller OH-ioner.
* Imidlertid forbliver salten i sig selv en neutral forbindelse.
Som konklusion er makroskopiske prøver af salte neutrale forbindelser på grund af fuldstændig overførsel af elektroner i ionisk binding, hvilket resulterer i en afbalanceret fordeling af positive og negative ladninger inden for krystalgitteret.
Sidste artikelEr pH 9 i vaskeri flydende god?
Næste artikelHvilke er mere destruktive kropsbølger eller overfladebølger?
 Varme artikler
Varme artikler
-
 En hurtig, letanvendelig DNA-amplifikationsmetode ved 37 CelciusEn DNA-streng (lilla) primer eksponentiel amplifikation af DNA (rød) som signaler til at dirigere lysemission af DNA-nanodevices. Kredit:Organisk og biomolekylær kemi Forskere i Japan har udviklet
En hurtig, letanvendelig DNA-amplifikationsmetode ved 37 CelciusEn DNA-streng (lilla) primer eksponentiel amplifikation af DNA (rød) som signaler til at dirigere lysemission af DNA-nanodevices. Kredit:Organisk og biomolekylær kemi Forskere i Japan har udviklet -
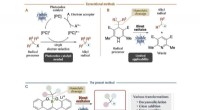 Ny protokol for organisk syntese ved hjælp af organoboronforbindelser og synligt lysSammenligning af konventionelle metoder og den foreliggende metode Credit:Kanazawa University Alkylradikaler er carbonradikaler af normale og forgrenede alkaner, tilgængelig som reaktionsmellempro
Ny protokol for organisk syntese ved hjælp af organoboronforbindelser og synligt lysSammenligning af konventionelle metoder og den foreliggende metode Credit:Kanazawa University Alkylradikaler er carbonradikaler af normale og forgrenede alkaner, tilgængelig som reaktionsmellempro -
 Et hjertesundt protein fra klid af kornafgrøderKredit:CC0 Public Domain Rævehale hirse er et etårigt græs, der dyrkes bredt som en kornafgrøde i dele af Indien, Kina og Sydøstasien. Maling af kornet fjerner det hårde ydre lag, eller klid, fra
Et hjertesundt protein fra klid af kornafgrøderKredit:CC0 Public Domain Rævehale hirse er et etårigt græs, der dyrkes bredt som en kornafgrøde i dele af Indien, Kina og Sydøstasien. Maling af kornet fjerner det hårde ydre lag, eller klid, fra -
 Polymer termisk regulator omdannes fra leder til isolator og tilbage igenDen rotationsforstyrrede sekskantede fase. Kredit:College of Engineering Polymerer bruges til at udvikle forskellige materialer, såsom plastik, nylon og gummi. I deres mest grundlæggende form, de
Polymer termisk regulator omdannes fra leder til isolator og tilbage igenDen rotationsforstyrrede sekskantede fase. Kredit:College of Engineering Polymerer bruges til at udvikle forskellige materialer, såsom plastik, nylon og gummi. I deres mest grundlæggende form, de
- 30% af Californiens jord skal bevares under ny ordre fra Gov. Newsoms
- Sådan bruges krystaller til at generere Electricity
- Røg fra naturbrande afslører årtiers luftkvalitetsgevinster
- Sporing af varmedrevet henfald i førende elektriske bilbatterier
- Hvilken planet har permanente storme?
- Rumvandrende astronauter tjekker stedet for kapsellækage


