Hvordan bruges temperatur til at genkende en faseændring?
* opvarmning af et stof: Når du tilføjer varmeenergi til et stof, stiger dens temperatur. Denne energi absorberes af molekylerne, hvilket får dem til at bevæge sig hurtigere og vibrere mere intenst.
* når faseændringspunktet: Ved en specifik temperatur bruges den tilsatte energi ikke længere til at øge molekylernes kinetiske energi, men til at bryde bindingerne mellem dem. Dette er faseændringspunktet.
* faseovergang: Under faseændringen forbliver temperaturen konstant, selvom der stadig tilsættes varme. Dette skyldes, at energien bruges til at overvinde de intermolekylære kræfter, ikke til at øge temperaturen.
* Ny fase: Når faseændringen er afsluttet, begynder temperaturen at stige igen, da energien bruges til at øge molekylernes kinetiske energi i den nye fase.
Eksempler:
* smeltning: Når du opvarmer is, stiger dens temperatur, indtil den når 0 ° C (32 ° F). På dette tidspunkt begynder isen at smelte, og temperaturen forbliver konstant ved 0 ° C, indtil al isen er blevet vand.
* kogning: Når du opvarmer vand, stiger dens temperatur, indtil den når 100 ° C (212 ° F). På dette tidspunkt begynder vandet at koge, og temperaturen forbliver konstant ved 100 ° C, indtil alt vandet er blevet til damp.
Vigtige punkter:
* Den temperatur, hvormed en faseændring opstår, kaldes faseændringspunktet .
* Faseændringspunktet er en karakteristisk egenskab for et stof.
* Temperaturen forbliver konstant under en faseændring, fordi den tilsatte energi bruges til at bryde intermolekylære bindinger i stedet for at øge kinetisk energi.
Derfor kan vi ved at overvåge temperaturen på et stof, når det opvarmes eller afkøles, identificere faseændringspunkterne og bestemme det fase, stoffet er i.
Sidste artikelHvilke faktorer bestemmer den metode, der bruges til at udtrække et metal?
Næste artikelHvad menes med protonnummer?
 Varme artikler
Varme artikler
-
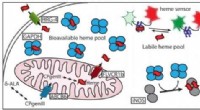 Hvordan celler håndterer en klæbrig, giftig, men absolut essentielt molekyleEt nyligt papir beskriver, hvordan hæm er chaperoneret til dets målproteiner. Kredit:Dennis Stuehr, Cleveland Clinic Nyder du at trække vejret? Du bør spare en tanke en gang imellem for heme, et j
Hvordan celler håndterer en klæbrig, giftig, men absolut essentielt molekyleEt nyligt papir beskriver, hvordan hæm er chaperoneret til dets målproteiner. Kredit:Dennis Stuehr, Cleveland Clinic Nyder du at trække vejret? Du bør spare en tanke en gang imellem for heme, et j -
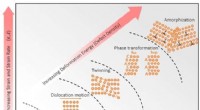 Øer uden struktur inde i metallegeringer kan føre til hårdere materialerForeslået hierarkisk deformationsmekanisme-paradigme for de ækviatomiske CrCoNi-baserede HEAer udsat for stigende grader af deformation. Elastisk deformation, dislokationsmedieret plasticitet, twinnin
Øer uden struktur inde i metallegeringer kan føre til hårdere materialerForeslået hierarkisk deformationsmekanisme-paradigme for de ækviatomiske CrCoNi-baserede HEAer udsat for stigende grader af deformation. Elastisk deformation, dislokationsmedieret plasticitet, twinnin -
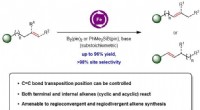 Manipulerer kædevandring i olefiner ved hjælp af jord-rigelige jernbaserede katalysatorerFigur 1:Skematisk viser migration af C =C -bindingen i alkener kan opnås ved hjælp af jernkatalyse med mindre end støkiometriske mængder af en base og borylreagens. Kredit: Journal of the American Che
Manipulerer kædevandring i olefiner ved hjælp af jord-rigelige jernbaserede katalysatorerFigur 1:Skematisk viser migration af C =C -bindingen i alkener kan opnås ved hjælp af jernkatalyse med mindre end støkiometriske mængder af en base og borylreagens. Kredit: Journal of the American Che -
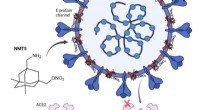 Nyt lægemiddel har potentiale til at vende SARS-CoV-2-virus mod sig selvEt lægemiddel udviklet af Scripps Research-forskere forhindrer SARS-CoV-2 (blå) i at binde sig til ACE2-receptorer (lyserøde) for at inficere menneskelige celler. Lægemidlet hæfter sig på virussen og
Nyt lægemiddel har potentiale til at vende SARS-CoV-2-virus mod sig selvEt lægemiddel udviklet af Scripps Research-forskere forhindrer SARS-CoV-2 (blå) i at binde sig til ACE2-receptorer (lyserøde) for at inficere menneskelige celler. Lægemidlet hæfter sig på virussen og
- Nye økologiske kort viser en bredere vifte af funktionel mangfoldighed
- Hvorfor skulle brug af en lille køkkenapparatstur Circuit Breaker til soveværelser og ikke afsætn…
- Forskere opdager, hvordan dødelige biofilm dannes
- GOP vs. ESG:Hvorfor Floridas guvernør Ron DeSantis, republikanere kæmper mod 'vågne' ESG-invester…
- En innovativ proces forhindrer irreversibelt energitab i batterier
- I hvilket land står solen sidst op?


