Hvorfor er anden elektronaffinitet for halogener nul?
* Elektronaffinitet (EA): Elektronaffinitet er den energiændring, der opstår, når et elektron tilsættes til et neutralt gasformigt atom til at danne en negativ ion.
* Første elektronaffinitet: Generelt har halogener meget høje første elektronaffiniteter, fordi de har en stærk attraktion for en ekstra elektron til at afslutte deres octet og opnå en stabil ædelgaskonfiguration.
* anden elektronaffinitet: Efter at have fået en elektron bliver halogener negativt ladede ioner (halogenidioner). At tilføje en anden elektron til en negativt ladet ion er ugunstig På grund af elektrostatisk frastødelse. Imidlertid er denne frastødelse ikke så stærk som tiltrækningen mellem den positivt ladede kerne og den negativt ladede elektron.
* Hvorfor den anden elektronaffinitet er negativ: På trods af afvisningen er den anden elektronaffinitet for halogener stadig negativ, fordi den frigivne energi, når den anden elektron tilsættes, er større end den energi, der kræves for at overvinde den elektrostatiske frastødelse.
Kortfattet:
* Den anden elektronaffinitet for halogener er negativ (ikke nul) på grund af den stærke tiltrækning af kernen for den indkommende elektron, selvom der er elektrostatisk frastødning fra den eksisterende negative ladning.
* Størrelsen af den anden elektronaffinitet for halogener er meget mindre end den første elektronaffinitet på grund af den elektrostatiske frastødelse.
Det er vigtigt at bemærke, at den anden elektronaffinitet altid er mindre negativ end den første elektronaffinitet for alle elementer.
Sidste artikelHvad er en korrekt beskrivelse af entalpi -reaktionen?
Næste artikelOrganisk molekyle klassificeres som et kulhydrat?
 Varme artikler
Varme artikler
-
 Gennembrud i forståelsen af enzymer, der laver antibiotika til lægemiddelresistent patogenProf Józef Lewandowski udfører nuklear magnetisk resonansspektroskopi, en nøgleteknikker brugt i arbejdet. Kredit:University of Warwick En af WHOs tre kritiske prioriterede patogener, Acinetobacte
Gennembrud i forståelsen af enzymer, der laver antibiotika til lægemiddelresistent patogenProf Józef Lewandowski udfører nuklear magnetisk resonansspektroskopi, en nøgleteknikker brugt i arbejdet. Kredit:University of Warwick En af WHOs tre kritiske prioriterede patogener, Acinetobacte -
 Knækker koden for et formskiftende proteinKredit:Pixabay/CC0 Public Domain Et formskiftende immunsystemprotein kaldet XCL1 udviklede sig fra en enkelt-formede forfader for hundreder af millioner af år siden. Nu, forskere ved Medical Colle
Knækker koden for et formskiftende proteinKredit:Pixabay/CC0 Public Domain Et formskiftende immunsystemprotein kaldet XCL1 udviklede sig fra en enkelt-formede forfader for hundreder af millioner af år siden. Nu, forskere ved Medical Colle -
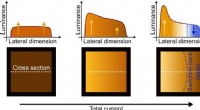 Hot OLED'er kan skifte tilbageBevis for tilbagekoblede områder ved at detektere luminansændringer i OLEDer:Den nederste linje af figuren præsenterer top-view-skitserne på en OLED-pixel ved tre forskellige eksemplariske stadier af
Hot OLED'er kan skifte tilbageBevis for tilbagekoblede områder ved at detektere luminansændringer i OLEDer:Den nederste linje af figuren præsenterer top-view-skitserne på en OLED-pixel ved tre forskellige eksemplariske stadier af -
 En mere følsom enhed til karakterisering af DNA i blodcirkulationenPrincippet for BIABoosters analysesystem. Fra en renset plasmaprøve, 1 µL analyseres med BIABooster-enheden, som koncentrerer sig, adskiller og detekterer størrelsesprofilen af det cirkulerende DNA.
En mere følsom enhed til karakterisering af DNA i blodcirkulationenPrincippet for BIABoosters analysesystem. Fra en renset plasmaprøve, 1 µL analyseres med BIABooster-enheden, som koncentrerer sig, adskiller og detekterer størrelsesprofilen af det cirkulerende DNA.
- Partikler fra dagligdags vægmaling kan skade levende organismer, men en ny membran viser høje filt…
- Sporer hacks automatisk, før hackerne gør det
- Forbedret model for massefordelingen af galaksehoben SMACS J0723.3−7327 baseret på Webb-teleskopb…
- Hvordan bakterier binder deres usynlighedskapper til immunforsvaret
- Er jern er et rent stof eller en blanding?
- Snapchat -forælder presset af fald i brugere


