Hvorfor har bicarbonat af soda alkali?
* Hydrolyse: Når natriumbicarbonat opløses i vand, gennemgår det hydrolyse. Dette betyder, at det reagerer med vandmolekyler til at producere hydroxidioner (OH⁻), som er ansvarlige for den alkaliske natur af en opløsning.
* reaktion: Nahco₃ + h₂o ⇌ h₂co₃ + naoh
* Reaktionen er i ligevægt, hvilket betyder, at den går i begge retninger.
* Dannelsen af NaOH (natriumhydroxid) er en stærk base, hvilket fører til frigivelse af OH⁻ioner.
* ph: En opløsning af natriumbicarbonat vil have en pH -værdi større end 7, hvilket indikerer alkalinitet. Dette skyldes tilstedeværelsen af hydroxidioner (OH⁻) i opløsningen.
Kortfattet:
Bicarbonat af soda udviser alkaliske egenskaber på grund af frigivelse af hydroxidioner (OH⁻), når det opløses i vand. Disse ioner neutraliserer syrer, hvorfor natriumbicarbonat ofte bruges som et antacida eller i bagning for at neutralisere sure ingredienser.
Sidste artikelHvad er små dråber væske ophængt i luften fra?
Næste artikelIndeholder alle forbindelser mindst et element?
 Varme artikler
Varme artikler
-
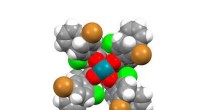 Nye syntesemetoder forbedrer 3-D kemisk plads til lægemiddelopdagelseGrafisk viser den udviklede dirhodium-katalysator, der bruges til at syntetisere et 3D-stillads af stor interesse for den farmaceutiske industri. Davies-laboratoriet har udgivet en række store artikle
Nye syntesemetoder forbedrer 3-D kemisk plads til lægemiddelopdagelseGrafisk viser den udviklede dirhodium-katalysator, der bruges til at syntetisere et 3D-stillads af stor interesse for den farmaceutiske industri. Davies-laboratoriet har udgivet en række store artikle -
 Ny katalysator hjælper med at omdanne kuldioxid til brændstofAisulu Aitbekova, venstre, og Matteo Cargnello foran reaktoren, hvor Aitbekova udførte mange af eksperimenterne til dette projekt. Kredit:L.A. Cicero Forestil dig at få fat i kuldioxid fra bilers
Ny katalysator hjælper med at omdanne kuldioxid til brændstofAisulu Aitbekova, venstre, og Matteo Cargnello foran reaktoren, hvor Aitbekova udførte mange af eksperimenterne til dette projekt. Kredit:L.A. Cicero Forestil dig at få fat i kuldioxid fra bilers -
 Bærbart kemisæt giver mulighed for testning af bushfoods sødme på stedetUdstyr i kemi værktøjskasse. Kredit:Coopers Plains Labs juni 2021 Oprindelige samfund kan nu vurdere kvaliteten og sødmen af deres vildt høstede indfødte buskfrugter i marken, i stedet for at se
Bærbart kemisæt giver mulighed for testning af bushfoods sødme på stedetUdstyr i kemi værktøjskasse. Kredit:Coopers Plains Labs juni 2021 Oprindelige samfund kan nu vurdere kvaliteten og sødmen af deres vildt høstede indfødte buskfrugter i marken, i stedet for at se -
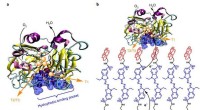 Forbedring af elektronoverførsel i enzymatiske biobrændselscellerDen som designet poly(pyrr)–ABTS–pyr film. en, Repræsentationer af Trametes versicolor Lac med den hydrofobe bindingslomme orienteret mod bunden af siden og T1 kobberstedet placeret på den ene side
Forbedring af elektronoverførsel i enzymatiske biobrændselscellerDen som designet poly(pyrr)–ABTS–pyr film. en, Repræsentationer af Trametes versicolor Lac med den hydrofobe bindingslomme orienteret mod bunden af siden og T1 kobberstedet placeret på den ene side
- Atomiske Nummer Vs. Smeltepunkter
- Seismisk risikovurdering af Campotosto, Italien
- Polymer science team designer ny nanoteknisk teknik til billigere materialereparation
- At skelne mellem beskrivende og årsagsundersøgelser
- NASA håber, at opsendelsen i New Zealand vil bane vejen for månelanding
- Hvorfor bruger forskere værktøjer, når de foretager observationer?


