Hvad er oxidationshalvreaktionen for 2 mg plus O2 lig med 2mgo?
2 mg + o₂ → 2 mgo
1. Identificer oxidation og reduktion:
* Oxidation: Magnesium (Mg) mister elektroner og går fra en oxidationstilstand på 0 til +2 i MgO.
* reduktion: Oxygen (O) får elektroner og går fra en oxidationstilstand på 0 i O₂ til -2 i MgO.
2. Skriv halvreaktionen for oxidation:
Oxidationen halvreaktion fokuserer på de arter, der oxideres (mg):
mg → mg²⁺ + 2e⁻
Forklaring:
* mg er magnesiumatomet i sin elementære form.
* mg²⁺ er magnesiumion, der har mistet to elektroner.
* 2e⁻ Repræsenterer de to elektroner, der blev tabt under oxidation.
Vigtig note: Du skal afbalancere både atomerne og ladningen på hver side af halvreaktionen.
Sidste artikelHvordan adskiller diffusion af gasser sig i dag og natplanter?
Næste artikelHvad er C28H58 plus O2?
 Varme artikler
Varme artikler
-
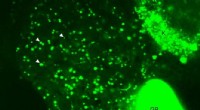 Forskere ser fedtstofskiftet i levende fisk, observere lipidbiokemi i realtidEt levende billede af leveren af en gennemskinnelig, larve zebrafisk. Det er taget ved hjælp af konfokal mikroskopi, som giver mulighed for klare billeder af de indre organer af et helt levende dyr.
Forskere ser fedtstofskiftet i levende fisk, observere lipidbiokemi i realtidEt levende billede af leveren af en gennemskinnelig, larve zebrafisk. Det er taget ved hjælp af konfokal mikroskopi, som giver mulighed for klare billeder af de indre organer af et helt levende dyr. -
 Forskere skaber nye kemiske næser for at befri miljøet for industrielle forurenende stofferTegneseriebillede af den kemiske næse. Kredit:Prof Riina Aav Forskere fra fem europæiske lande er gået sammen om at udvikle næste generations kemiske næser for at fjerne industrielle forurenende s
Forskere skaber nye kemiske næser for at befri miljøet for industrielle forurenende stofferTegneseriebillede af den kemiske næse. Kredit:Prof Riina Aav Forskere fra fem europæiske lande er gået sammen om at udvikle næste generations kemiske næser for at fjerne industrielle forurenende s -
 Udvikling af elektrodemateriale, der forbedrer effektiviteten af saltholdighedsgradientenergiVed anvendelse af omvendt elektrodialysesystem (a) Effekttæthed (b) Strømspændingskurve (c) Modstand (d) Princip for strømgenerering (e og f) Elektrokemisk reaktion og elektronoverførselsprincip ved e
Udvikling af elektrodemateriale, der forbedrer effektiviteten af saltholdighedsgradientenergiVed anvendelse af omvendt elektrodialysesystem (a) Effekttæthed (b) Strømspændingskurve (c) Modstand (d) Princip for strømgenerering (e og f) Elektrokemisk reaktion og elektronoverførselsprincip ved e -
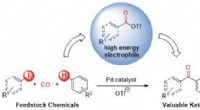 En grønnere måde at lave ketoner påKredit:McGill University Forskere ved McGill University har opdaget en ny, mere miljøvenlig måde at fremstille ketoner på, en vigtig kemisk ingrediens i lægemidler. Mens ketoner findes i en lang r
En grønnere måde at lave ketoner påKredit:McGill University Forskere ved McGill University har opdaget en ny, mere miljøvenlig måde at fremstille ketoner på, en vigtig kemisk ingrediens i lægemidler. Mens ketoner findes i en lang r
- Undgå bobleproblemer:Undersøgelse af forholdet mellem bobler og elektrokemi
- Kemikere lukker hullet i at gøre nanomedicin sikrere, mere effektivt
- Et kvantespring for ultrapræcis måling og informationskodning?
- Lavpris grafen-jern-filtre, der selektivt adskiller gasblandinger
- Hvordan neandertalersprog adskilte sig fra moderne mennesker - de brugte sandsynligvis ikke metafore…
- Keck Observatory planet imager leverer første videnskab


