Hvilken familie af elementer mister mest elektroner?
Her er hvorfor:
* Elektronisk konfiguration: Alkalimetaller har kun en valenselektron i deres yderste skal.
* lav ioniseringsenergi: De har en relativt lav ioniseringsenergi, hvilket betyder, at det kræver mindre energi at fjerne den enkelt valenselektron.
* Elektropositivitet: Alkalimetaller er meget elektropositive, hvilket betyder, at de har en stærk tendens til at miste elektroner og danne positive ioner (kationer).
Eksempel: Natrium (NA) mister let sin ene valenselektron for at danne en Na+ -ion.
Fortæl mig, hvis du gerne vil have flere detaljer om nogen af disse koncepter!
Sidste artikelHvilke materialer bruges i pulverbelægning?
Næste artikelHvad betyder NIE i kemi?
 Varme artikler
Varme artikler
-
 Fremstilling af F-18 radiofarmaka til PET-billeddannelseKredit:CC0 Public Domain For nylig har ANSTO-forskere gjort fremskridt med at undersøge forbedrede måder at lave livreddende radiofarmaka på ved hjælp af fluor-18 radioisotopen, så de kan fås på f
Fremstilling af F-18 radiofarmaka til PET-billeddannelseKredit:CC0 Public Domain For nylig har ANSTO-forskere gjort fremskridt med at undersøge forbedrede måder at lave livreddende radiofarmaka på ved hjælp af fluor-18 radioisotopen, så de kan fås på f -
 Frigørelse af svovls kraft i fremtidigt lægemiddeldesignKredit:UTSA Organiske svovlforbindelser er udbredt til stede i vores kroppe og det naturlige miljø. De findes i løg, skalotteløg og endda blomkål. Medicinsk forskning viser, at når det indtages, d
Frigørelse af svovls kraft i fremtidigt lægemiddeldesignKredit:UTSA Organiske svovlforbindelser er udbredt til stede i vores kroppe og det naturlige miljø. De findes i løg, skalotteløg og endda blomkål. Medicinsk forskning viser, at når det indtages, d -
 Kombinatorisk high-throughput-strategi foreslået til screening af hydrogenudviklingsreaktionskataly…Skematisk illustration af high-throughput boble screeningsmetode. Kredit:NIMTE En forskergruppe ledet af prof. Wang Junqiang ved Ningbo Institute of Materials Technology and Engineering (NIMTE) und
Kombinatorisk high-throughput-strategi foreslået til screening af hydrogenudviklingsreaktionskataly…Skematisk illustration af high-throughput boble screeningsmetode. Kredit:NIMTE En forskergruppe ledet af prof. Wang Junqiang ved Ningbo Institute of Materials Technology and Engineering (NIMTE) und -
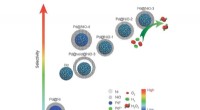 Interface engineering core@shell nanopartikler til aktiv og selektiv direkte H2O2-genereringSkematisk illustration, der viser aktiviteten og selektiviteten over for H2O2-syntese af 5 vægt% Pd@Ni-3/TiO2, 5 vægt% Pd@NiO-x/TiO2 (x =1, 2, 3, 4), 5 vægt% Pd@void@Ni-3/TiO2 og 5 vægt% Pd/Ti02. Kred
Interface engineering core@shell nanopartikler til aktiv og selektiv direkte H2O2-genereringSkematisk illustration, der viser aktiviteten og selektiviteten over for H2O2-syntese af 5 vægt% Pd@Ni-3/TiO2, 5 vægt% Pd@NiO-x/TiO2 (x =1, 2, 3, 4), 5 vægt% Pd@void@Ni-3/TiO2 og 5 vægt% Pd/Ti02. Kred
- Landaftaler, der skal forbedre fødevaresikkerheden, kan have skadet
- Nanodiscs leverer personlig kræftbehandling til immunsystemet
- Om miljøbeskyttelse, Bidens-valget vil betyde en 180-graders vending fra Trumps politik
- Hvad er tåregas?
- Hvad vil der ske, hvis du bringer en ladet genstand nær en elektrisk neutral overflade?
- Hvorfor har planeter forskellige tidszoner?


