Gasser er gode isolatorer, fordi deres molekyler er?
Her er hvorfor:
* Afstand: Molekylerne i en gas er langt længere fra hinanden end i en væske eller fast stof. Dette betyder, at der er mindre mulighed for molekylerne til at kollidere og overføre varmeenergi.
* fri bevægelighed: Gasmolekyler bevæger sig tilfældigt rundt og har ikke faste positioner som faste stoffer eller væsker. Dette gør det vanskeligt for varme at overføre gennem gassen, fordi energien konstant spredes i tilfældige retninger.
I modsætning:
* faste stoffer: Molekyler er tæt pakket og vibrerer i faste positioner, hvilket muliggør effektiv varmeoverførsel.
* væsker: Molekyler er tættere sammen end i en gas, men har mere frihed til at bevæge sig, hvilket muliggør varmeoverførsel, men med mere modstand end i faste stoffer.
Tænk på det sådan:Forestil dig at prøve at skubbe en bold gennem en pakket skare. Det ville være meget sværere end at skubbe det gennem et felt med folk, der er fordelt langt fra hinanden!
Sidste artikelEr blanding af sand og salt klassificeret som heterogen eller homogen?
Næste artikelHvad er meget radioaktiv malm?
 Varme artikler
Varme artikler
-
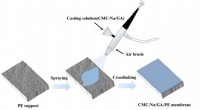 Pervaporationsmembraner viser løfte om genvinding af alkalisk spildevandEn (CMC-Na/GA)/PE-kompositmembran blev fremstillet ved spray-coating og viste fremragende egenskaber til alkalisk vandgenvinding. Kredit:Jianzhong Xia, Pei Li Industrielle processer genererer ofte
Pervaporationsmembraner viser løfte om genvinding af alkalisk spildevandEn (CMC-Na/GA)/PE-kompositmembran blev fremstillet ved spray-coating og viste fremragende egenskaber til alkalisk vandgenvinding. Kredit:Jianzhong Xia, Pei Li Industrielle processer genererer ofte -
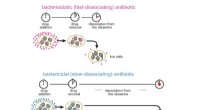 At lære antibiotika at være mere effektive dræbereForskning viser, at langvarig hæmning af proteinsyntese fører til celledød. Kredit:Proceedings of the National Academy of Sciences Forskning fra University of Illinois i Chicago tyder på bindingsv
At lære antibiotika at være mere effektive dræbereForskning viser, at langvarig hæmning af proteinsyntese fører til celledød. Kredit:Proceedings of the National Academy of Sciences Forskning fra University of Illinois i Chicago tyder på bindingsv -
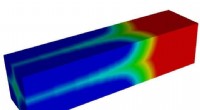 Undersøgelse afslører ukendte detaljer om almindelige lithium-ion batterimaterialerEn illustration viser væksten af en lithium-mangel fase (blå) på bekostning af en lithium-rig fase (rød) i en lithium jernfosfat mikrostav. Rice University-forskere ledede en undersøgelse, der fandt
Undersøgelse afslører ukendte detaljer om almindelige lithium-ion batterimaterialerEn illustration viser væksten af en lithium-mangel fase (blå) på bekostning af en lithium-rig fase (rød) i en lithium jernfosfat mikrostav. Rice University-forskere ledede en undersøgelse, der fandt -
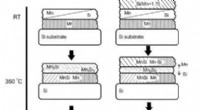 Fysikere overvåger dannelsen af film med højere mangansilicidSkematisk illustration af synteseproceduren til venstre:Mn17Si30 og højre Mn4Si7 -prøve. Kredit:Ivan Tarasov Et team fra Kirensky Institute of Physics (Siberian Branch of the Russian Academy of Sc
Fysikere overvåger dannelsen af film med højere mangansilicidSkematisk illustration af synteseproceduren til venstre:Mn17Si30 og højre Mn4Si7 -prøve. Kredit:Ivan Tarasov Et team fra Kirensky Institute of Physics (Siberian Branch of the Russian Academy of Sc
- Sentinel-satellit fanger fødslen af behemoth isbjerg
- Vigtigheden af kreativ problemløsning på arbejdspladsen
- Beskyttelse af hunde om vinteren mod ekstrem kulde, is, salt og tømidler
- Forskere skaber nyt smart nanokapsel-leveringssystem til brug i proteinterapi
- NASA hjælper med at advare om skadelige algeblomster i søer, reservoirer
- Hvad er eliminering i biologi?


