Hvad sker der med saltet i opløsning, efter at vand er fordampet?
* opløselighed: Salt opløses i vand, fordi vandmolekylerne omgiver saltioner, bryder de ioniske bindinger og holder dem i opløsning.
* Fordampning: Når vand fordamper, forlader vandmolekylerne opløsningen og efterlader saltionerne.
* Krystallisation: Efterhånden som mere vand fordamper, øges koncentrationen af saltioner. Til sidst bliver opløsningen mættet, hvilket betyder, at den ikke kan holde mere opløst salt. På dette tidspunkt begynder saltionerne at formere deres ioniske bindinger og krystalliseres ud af opløsningen og danner faste saltkrystaller.
Kort sagt: Saltet i opløsning forsvinder ikke, når vandet fordamper. Det forbliver bagud, enten opløst i det resterende vand eller som faste krystaller.
Sidste artikelHvad er den bedste analogi til fase fase?
Næste artikelForskellige typer krystalvækstteknikker?
 Varme artikler
Varme artikler
-
 Et enkelt enzym inducerer det kemiske forsvar af en svamp mod larverKredit:Wiley Nogle svampe producerer langkædede umættede carboxylsyrer som deres kemiske forsvar mod insektlarver. Biosyntesen af disse polyener er kun afhængig af ét enzym, som tyske videnskabs
Et enkelt enzym inducerer det kemiske forsvar af en svamp mod larverKredit:Wiley Nogle svampe producerer langkædede umættede carboxylsyrer som deres kemiske forsvar mod insektlarver. Biosyntesen af disse polyener er kun afhængig af ét enzym, som tyske videnskabs -
 En laserteknik viser sig effektiv til at genvinde materiale designet til at beskytte industriprodukt…Kredit:CC0 Public Domain Fluorpolymerer er makromolekyler, der består af carbon og fluor, som, på grund af deres egenskaber, tendens til at blive brugt som non-stick og antikorrosive belægninger p
En laserteknik viser sig effektiv til at genvinde materiale designet til at beskytte industriprodukt…Kredit:CC0 Public Domain Fluorpolymerer er makromolekyler, der består af carbon og fluor, som, på grund af deres egenskaber, tendens til at blive brugt som non-stick og antikorrosive belægninger p -
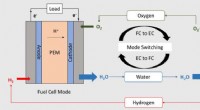 Ny katalysator hjælper med at kombinere brændselscelle, batteri i én enhedKredit:Washington University i St. Louis En enkelt enhed, der både genererer brændstof og oxidant fra vand og, når en kontakt drejes, omdanner brændstof og ilt til elektricitet og vand, har en ræk
Ny katalysator hjælper med at kombinere brændselscelle, batteri i én enhedKredit:Washington University i St. Louis En enkelt enhed, der både genererer brændstof og oxidant fra vand og, når en kontakt drejes, omdanner brændstof og ilt til elektricitet og vand, har en ræk -
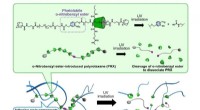 Vendbar klæbrighed i tandcement er noget at smile afKredit:Institut for Organiske Biomaterialer, TMDU Alle, der har fået fyldt tandhuller, ved, at de bedste tandmaterialer bliver, hvor tandlægen lægger dem. Vedhæftningen af i øjeblikket tilgængel
Vendbar klæbrighed i tandcement er noget at smile afKredit:Institut for Organiske Biomaterialer, TMDU Alle, der har fået fyldt tandhuller, ved, at de bedste tandmaterialer bliver, hvor tandlægen lægger dem. Vedhæftningen af i øjeblikket tilgængel
- Er nitrogenoxider skadelige for miljøet?
- Hvilke elbiler kvalificerer sig til ny amerikansk skattefradrag? Websteder tilbyder hjælp
- Hvad er en organisme, der springer, når et skarpt lys lyste på den?
- Lys et lys i stedet for at skifte batteri
- Hvor er det tørreste sted på jorden?
- Hvorfor er Bluebird Days fantastiske for skiløbere og dårlige jægere?


