Hvad sker der med et volumen gas, når temperaturen reduceres?
Her er hvorfor:
* kinetisk molekylær teori: Den kinetiske molekylære teori siger, at gasmolekyler er i konstant tilfældig bevægelse, og deres gennemsnitlige kinetiske energi er direkte proportional med den absolutte temperatur.
* Nedsat temperatur, nedsat kinetisk energi: Når temperaturen falder, falder den gennemsnitlige kinetiske energi for gasmolekylerne. Dette betyder, at de bevæger sig langsommere.
* mindre kollisioner: Langsomere molekyler kolliderer sjældnere med beholderens vægge.
* reduceret tryk: Nedsatte kollisioner betyder mindre tryk, der udøves på containervæggene.
* Volumenkontraktion: For at opretholde et konstant tryk skal gassens volumen falde for at kompensere for det reducerede antal kollisioner.
Dette forhold mellem temperatur og volumen opsummeres af Charles lov :
v₁/t₁ =v₂/t₂
Hvor:
* V₁ er det oprindelige bind
* T₁ er den oprindelige temperatur
* V₂ er det endelige bind
* T₂ er den endelige temperatur
Vigtig note: Dette forhold gælder kun, hvis trykket og mængden af gas forbliver konstant.
Sidste artikelHvad sker der med bevægelsen af molekyler, når deres temperatur er?
Næste artikelHvad gør benzalkonium?
 Varme artikler
Varme artikler
-
 Nye fund om effekten af Epsom salt - Epsom salt receptor identificeretModelpræsentation af den humane bitre receptor TAS2R7, også kendt som Epsom salt receptor. Kredit:Dr. Antonella Di Pizio / Leibniz-LSB@TUM Tyskland Et team af videnskabsmænd ledet af Maik Behrens
Nye fund om effekten af Epsom salt - Epsom salt receptor identificeretModelpræsentation af den humane bitre receptor TAS2R7, også kendt som Epsom salt receptor. Kredit:Dr. Antonella Di Pizio / Leibniz-LSB@TUM Tyskland Et team af videnskabsmænd ledet af Maik Behrens -
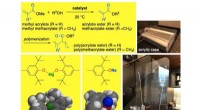 Industriel forbindelse får en miljøvenlig reaktionNatrium- eller magnesiumaryloxider kan katalysere transesterificeringen af methyl(meth)acrylat ved stuetemperatur, med høj kemoselektivitet, producerer et højt udbytte af (meth) acrylatester, og ude
Industriel forbindelse får en miljøvenlig reaktionNatrium- eller magnesiumaryloxider kan katalysere transesterificeringen af methyl(meth)acrylat ved stuetemperatur, med høj kemoselektivitet, producerer et højt udbytte af (meth) acrylatester, og ude -
 Sporing af atombevægelse i realtid mellem krystalkorn i metallerTing Zhu, professor i maskinteknik ved Georgia Tech, foran sine TEM-billeder af polykrystallinske metaller og en grafisk simulerende atomstruktur. Kredit:Georgia Tech Metalliske materialer, der bru
Sporing af atombevægelse i realtid mellem krystalkorn i metallerTing Zhu, professor i maskinteknik ved Georgia Tech, foran sine TEM-billeder af polykrystallinske metaller og en grafisk simulerende atomstruktur. Kredit:Georgia Tech Metalliske materialer, der bru -
 Forskning finder, at mekanisk drevet kemi accelererer reaktioner i sprængstofferKredit:Pixabay/CC0 Public Domain Forskere ved Lawrence Livermore National Laboratory (LLNL) Energetic Materials Center og Purdue University Materials Engineering Department har brugt simuleringer u
Forskning finder, at mekanisk drevet kemi accelererer reaktioner i sprængstofferKredit:Pixabay/CC0 Public Domain Forskere ved Lawrence Livermore National Laboratory (LLNL) Energetic Materials Center og Purdue University Materials Engineering Department har brugt simuleringer u
- Is former jordskredlandskabet på Mars
- Hvorfor eksisterer materie? Afrunding af elektroner kan indeholde spor
- Emissioner af forbudt ozonædende kemikalie stiger på en eller anden måde
- Sydkorea tester levering af droner i fjerntliggende regioner
- Varmen er tændt:Hvad vi ved om, hvorfor havtemperaturer bliver ved med at smadre rekorder
- Forskere undersøger drivende faktorer, der påvirker bæredygtigheden af endorheiske regioner


