Hvorfor er glas en væske?
Her er en sammenbrud:
hvorfor glas ikke er en væske:
* Mangel på defineret struktur: Væsker har molekyler arrangeret i et tilfældigt, konstant skiftende mønster. Glas, der optræder amorf, har et mere struktureret arrangement af molekyler tættere på et fast stof.
* Ingen strøm over tid: Væsker flyder over tid på grund af deres molekylære mobilitet. Glas flyder ikke ved stuetemperatur; Det er utroligt tyktflydende.
* smeltepunkt: Væsker har et specifikt smeltepunkt, hvor de skifter fra fast til væske. Glas blødgør gradvist over en række temperaturer og smelter ikke på et specifikt punkt.
Hvorfor den "flydende" misforståelse findes:
* Viskositet: Glas er et ekstremt tyktflydende stof. Dette betyder, at det flyder utroligt langsomt, hvilket får det til at virke som en meget langsomt bevægende væske over utroligt lange perioder. Dette er tydeligt i meget gamle glasvinduer, hvor den nederste del kan forekomme tykkere end toppen.
* amorf struktur: Glas har ikke den regelmæssige, krystallinske struktur af de fleste faste stoffer. Denne mangel på orden kan være forvirrende.
Kortfattet:
Glas er et ikke-krystallinsk fast stof med ekstremt høj viskositet, hvilket får den til at opføre sig som en væske over ekstremt lange tidsskalaer. Det er dog ikke teknisk en væske.
Sidste artikelFunktioner af spatel i laboratorieapparater?
Næste artikelHvad danner store molekyler fra mindre?
 Varme artikler
Varme artikler
-
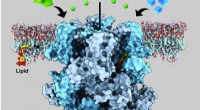 Form af struktur, som nerveceller bruger til at fornemme kulde og menthol, kunne være et nyt mål f…En ionkanal i humane nerveceller kaldet det forbigående receptorpotentielle melastatinelement 8 (TRPM8) registrerer både kulde og menthol, overføre kølende fornemmelser ved at frigive calcium (grønne
Form af struktur, som nerveceller bruger til at fornemme kulde og menthol, kunne være et nyt mål f…En ionkanal i humane nerveceller kaldet det forbigående receptorpotentielle melastatinelement 8 (TRPM8) registrerer både kulde og menthol, overføre kølende fornemmelser ved at frigive calcium (grønne -
 Ny forskning afslører hemmelighederne bag fotosyntesen, der kan hjælpe med at udvikle computertekn…Illustrerer, hvordan destinationen for en elektron (repræsenteret af toget) kan dirigeres efter påføring af en ultrahurtig mid-infrarød puls (repræsenteret af ilden). Kredit:Helen Towrie ved CLF F
Ny forskning afslører hemmelighederne bag fotosyntesen, der kan hjælpe med at udvikle computertekn…Illustrerer, hvordan destinationen for en elektron (repræsenteret af toget) kan dirigeres efter påføring af en ultrahurtig mid-infrarød puls (repræsenteret af ilden). Kredit:Helen Towrie ved CLF F -
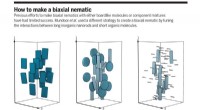 En ny måde at lave biaksiale nematisk fase flydende krystaller påSådan laver du en biaksial nematisk. Tidligere bestræbelser på at fremstille biaksiale nematik med enten bordlignende molekyler eller komponentblandinger har haft begrænset succes. Mundoor et al. brug
En ny måde at lave biaksiale nematisk fase flydende krystaller påSådan laver du en biaksial nematisk. Tidligere bestræbelser på at fremstille biaksiale nematik med enten bordlignende molekyler eller komponentblandinger har haft begrænset succes. Mundoor et al. brug -
 Forskere er pionerer på en grønnere måde at skabe sammenvævede polymerer med blåt lysUniversity of Delaware forskere lavede universitetets logo ved hjælp af deres nyudviklede polymerisationsteknik. Kredit:Abhishek Shete/ University of Delaware Et par ingeniører ved University of D
Forskere er pionerer på en grønnere måde at skabe sammenvævede polymerer med blåt lysUniversity of Delaware forskere lavede universitetets logo ved hjælp af deres nyudviklede polymerisationsteknik. Kredit:Abhishek Shete/ University of Delaware Et par ingeniører ved University of D
- Finjuster enhedens ydeevne med sværme af svømmeceller
- Sådan læser du Decimal Place Value
- Hvilken tilpasning gjorde det muligt for gymnospermplanter at kolonisere og dominere jord?
- Sådan optimerer du processen med polymerekstrudering
- Hvad er det græske kemiord?
- Bystørrelse spiller en afgørende rolle i migrationsmønstre


