Hvilke andre ting opløses i vand?
opløselige forbindelser:
* salte: De fleste salte, som bordsalt (NaCl), opløses let i vand.
* sukker: Enkle sukkerarter som glukose og fruktose opløses let.
* syrer: Mange syrer, såsom saltsyre (HCI) og svovlsyre (H₂so₄), er meget opløselige i vand.
* baser: Mange baser, som natriumhydroxid (NaOH) og kaliumhydroxid (KOH), er også meget opløselige.
* ethanol: Alkohol, som ethanol, er blandbar med vand, hvilket betyder, at de kan blande i enhver andel.
Faktorer, der påvirker opløselighed:
* Polaritet: Vand er et polært molekyle (den ene ende er lidt positivt, den anden lidt negativ). Stoffer med lignende polaritet som vand, som salte og sukker, opløses godt. Ikke -polære stoffer, som olier, gør det ikke.
* Temperatur: Generelt øger stigende temperaturopløselighed for de fleste faste stoffer.
* tryk: Tryk har en betydelig indflydelse på opløseligheden af gasser i væsker. Højere tryk øger opløseligheden.
Eksempler på almindelige stoffer, der opløses i vand:
* salt (NaCl)
* sukker (c₁₂h₂₂o₁₁)
* eddike (eddikesyre)
* bagepulver (natriumbicarbonat)
* sæbe
* vaskemiddel
* kaffe
* te
* juice
* Mange medicin
ting, der ikke opløses i vand:
* olier og fedt (ikke -polær)
* sand
* plast
* træ
Husk: Opløsning er en kompleks proces, der er påvirket af mange faktorer. Nogle stoffer opløses kun delvist og danner løsninger med en grænse for, hvor meget opløst stof kan opløses ved en given temperatur.
Sidste artikelHvad sker der, når du blander citronsyre bagepulver og eddike?
Næste artikelHvad er opløsningsmiddel og opløsning?
 Varme artikler
Varme artikler
-
 Forskere skal undersøge, om metalkorroderende mikrober kan vokse i Canadas foreslåede atomaffaldsa…Kredit:Pixabay/CC0 Public Domain Med Canada tættere på at flytte alt sit brugte nukleare brændsel til en enkelt facilitet og indkapsle hver brændstofbeholder i bentonit-ler, studerer forskere, om d
Forskere skal undersøge, om metalkorroderende mikrober kan vokse i Canadas foreslåede atomaffaldsa…Kredit:Pixabay/CC0 Public Domain Med Canada tættere på at flytte alt sit brugte nukleare brændsel til en enkelt facilitet og indkapsle hver brændstofbeholder i bentonit-ler, studerer forskere, om d -
 Opdagelsen kan føre til bæredygtig ethanol fremstillet af kuldioxidAtomer på overfladen af kobber (751) er relativt langt fra hinanden sammenlignet med andre kobberkrystaller. Det kunne forklare, hvorfor kobber (751) er langt mere selektivt til at producere ethanol
Opdagelsen kan føre til bæredygtig ethanol fremstillet af kuldioxidAtomer på overfladen af kobber (751) er relativt langt fra hinanden sammenlignet med andre kobberkrystaller. Det kunne forklare, hvorfor kobber (751) er langt mere selektivt til at producere ethanol -
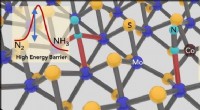 Ammoniaksyntese gjort let med 2-D katalysatorTilsætning af koboltatomer til fyldning af ledige pladser i 2D molybdendisulfidkrystaller øger materialets evne til at katalysere ammoniak fra dinitrogen. Forskere fra Rice University har udviklet en
Ammoniaksyntese gjort let med 2-D katalysatorTilsætning af koboltatomer til fyldning af ledige pladser i 2D molybdendisulfidkrystaller øger materialets evne til at katalysere ammoniak fra dinitrogen. Forskere fra Rice University har udviklet en -
 Opfindelse udløst af COVID-19-pandemi desinficerer overflader sikkert kontinuerligtKredit:Pixabay/CC0 Public Domain En opfindelse til at påføre plasma på genstande, der ofte berøres, til kontinuerlig desinfektion kunne give en sikker og effektiv, ikke-kemisk måde at reducere pat
Opfindelse udløst af COVID-19-pandemi desinficerer overflader sikkert kontinuerligtKredit:Pixabay/CC0 Public Domain En opfindelse til at påføre plasma på genstande, der ofte berøres, til kontinuerlig desinfektion kunne give en sikker og effektiv, ikke-kemisk måde at reducere pat
- Casimir-kraft bruges til at kontrollere og manipulere objekter
- Indsigt i vores 50-plus levetid, der stadig udvikler sig, genetisk undersøgelse viser
- Qatar, Exxon Mobil bygger et LNG -anlæg på $ 10 mia. I Texas
- Forskere håber, at nogle genstande overlevede Brasiliens museumsbrand
- Er der nogen vulkaner i Paris?
- Hvad er de vigtigste landformer og kroppe af vandkuba?


