Hvad ville et diagram over partikler i Gas State Show?
1. Bredt fordelt partikler: Gaspartikler er langt fra hinanden sammenlignet med deres størrelse. Dette skyldes, at de har en masse kinetisk energi og bevæger sig frit.
2. Tilfældig bevægelse: Partiklerne bevæger sig i tilfældige retninger og ved høje hastigheder. De kolliderer med hinanden og væggene i deres beholder.
3. Ingen fast volumen eller form: Da partiklerne er så langt fra hinanden, kan de let udvides til at fylde hele beholderen. De har ikke et bestemt volumen eller form.
Her er en simpel repræsentation:
Forestil dig en kasse. Inde i boksen tegner du små prikker (repræsenterer partiklerne) spredt over hele kassen. Prikkerne skal spredes ud, ikke samlet sammen.
For at gøre det endnu mere informativt kunne du:
* Tegn pile: Vis partiklernes tilfældige bevægelse ved at tilføje pile, der peger i forskellige retninger.
* Brug forskellige farver: Hvis du repræsenterer en blanding af gasser, skal du bruge forskellige farver til de forskellige partikler.
* Inkluder en note: Tilføj en note, der forklarer, at partiklerne ikke drages i skala og faktisk er meget mindre end det rum, de besætter.
Husk, at dette er en forenklet repræsentation. I virkeligheden bevæger gaspartikler konstant og kolliderer på en kompleks, kaotisk måde.
Sidste artikelStahl og Becher store bidrag til området kemi?
Næste artikelHvad er de fem dele af et godt designet eksperiment?
 Varme artikler
Varme artikler
-
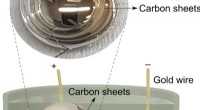 Flydende metaller nedbryder organiske brændstoffer til ultratynde grafitpladerKredit:University of New South Wales For første gang, forskere ved University of New South Wales (UNSW), Sydney, Australien, har demonstreret syntesen af ultratynde grafitiske materialer ved stu
Flydende metaller nedbryder organiske brændstoffer til ultratynde grafitpladerKredit:University of New South Wales For første gang, forskere ved University of New South Wales (UNSW), Sydney, Australien, har demonstreret syntesen af ultratynde grafitiske materialer ved stu -
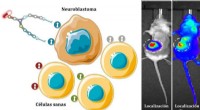 Syntetiske molekyler leverer lægemidler direkte til neuroblastomcellerKredit:Angewandte Chemie-International Edition 58 (2019) Forskere fra Universidad Politécnica de Madrid er involveret i udviklingen af specifikke molekylære stilladser, som er i stand til at lev
Syntetiske molekyler leverer lægemidler direkte til neuroblastomcellerKredit:Angewandte Chemie-International Edition 58 (2019) Forskere fra Universidad Politécnica de Madrid er involveret i udviklingen af specifikke molekylære stilladser, som er i stand til at lev -
 Forskere laver næste generation, batterikomponent med høj sejhedForskning viser, at grafen (rGO) kan hjælpe med at forhindre spredning af revner i keramiske materialer, der bruges til batterielektrolytter. Kredit:Brown University Et hold af Brown University-fo
Forskere laver næste generation, batterikomponent med høj sejhedForskning viser, at grafen (rGO) kan hjælpe med at forhindre spredning af revner i keramiske materialer, der bruges til batterielektrolytter. Kredit:Brown University Et hold af Brown University-fo -
 Kemisk katalysator forvandler affald til skat, gør inerte CH-bindinger reaktiveVi kan ændre et billigt og rigeligt kulbrinte med begrænset anvendelighed til et værdifuldt stillads til udvikling af nye forbindelser - såsom lægemidler og andre finkemikalier, siger J.T. Fu (ovenfo
Kemisk katalysator forvandler affald til skat, gør inerte CH-bindinger reaktiveVi kan ændre et billigt og rigeligt kulbrinte med begrænset anvendelighed til et værdifuldt stillads til udvikling af nye forbindelser - såsom lægemidler og andre finkemikalier, siger J.T. Fu (ovenfo
- Forskere demonstrerer transport af let last ved hjælp af tøjrede og ubundne bløde robotter lavet …
- Hvad er koncepterne om videnskabelig læsefærdighed?
- Starter børnehave på højre fod
- Afdækning af kriminalitetsmønstre ved hjælp af lokalitetsdata
- Hvordan kan metaller overholdes sammen ved hjælp af nitterings- og lodningsprocessen?
- Nye rammer tager højde for modstridende skøn over globale temperaturstigninger


