Hvad er funktionen af en saltbro i voltaisk celle?
1. Opretholdelse af elektrisk neutralitet:
* Elektrokemiske reaktioner: I en voltaisk celle forekommer oxidation ved anoden (elektroden, hvor elektroner frigøres), og reduktion forekommer ved katoden (elektroden, hvor elektroner opnås).
* ubalance: Disse reaktioner skaber en ubalance af ladning i cellen. Anodeopløsningen bliver mere positiv (på grund af tabet af elektroner), mens katodeløsningen bliver mere negativ (på grund af forstærkningen af elektroner).
* saltbroopløsning: Saltbroen indeholder en elektrolyt (en løsning, der leder elektricitet). Denne elektrolyt består normalt af ioner, der ikke let reagerer med elektroderne eller opløsningerne i cellen.
* ionisk strøm: Saltbroen giver ioner mulighed for at strømme fra den ene halvcelle til den anden og afbalancere ladningen. For eksempel, hvis anodopløsningen bliver positiv, vil negative ioner fra Salt Bridge migrere mod den. Tilsvarende, hvis katodeopløsningen bliver negativ, vil positive ioner fra Salt Bridge migrere mod den.
2. Afslutning af kredsløbet:
* Elektronstrøm: Elektroner strømmer fra anoden til katoden gennem et eksternt kredsløb.
* ionisk strøm: Saltbroen giver ioner mulighed for at strømme mellem halvcellerne og afslutte kredsløbet i cellen.
3. Forebyggelse af polarisering:
* polarisering: Når cellen fungerer, kan opbygningen af ladning på elektroderne hindre strømmen af strøm og forårsage polarisering.
* Salt Bridge -rolle: Saltbroen hjælper med at forhindre polarisering ved at opretholde ladningsneutralitet.
Kortfattet: Saltbroen i en voltaisk celle er vigtig for:
* Opretholdelse af elektrisk neutralitet i cellen.
* Færdiggør kredsløbet ved at tillade ionstrøm.
* Forebyggelse af polarisering af elektroderne.
Fortæl mig, hvis du har andre spørgsmål om voltaiske celler!
Sidste artikelHvordan måler du 3,2 oz olie?
Næste artikelHvad er den gas, der bruges i køleskab og klimaanlæg?
 Varme artikler
Varme artikler
-
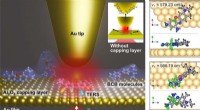 Iagttagelse af forskellen i strukturel dynamik af 1 nm enkeltmolekyler ved stuetemperatur for først…(Venstre) Illustration af isolerede molekyler fanget mellem guld- og aluminiumoxidlag ved hjælp af en spidsforstærket nanoskopi. (Højre) Visualisering af vibrationstilstandene for et brillant cresylbl
Iagttagelse af forskellen i strukturel dynamik af 1 nm enkeltmolekyler ved stuetemperatur for først…(Venstre) Illustration af isolerede molekyler fanget mellem guld- og aluminiumoxidlag ved hjælp af en spidsforstærket nanoskopi. (Højre) Visualisering af vibrationstilstandene for et brillant cresylbl -
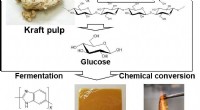 Den højeste varmebestandige plast nogensinde er udviklet af biomasseFigur 1. Udviklingsstrategi for cellulose-afledt PBI og PBI/PA film med ultrahøj termomodstand og rammehæmning. Kredit:Japan Advanced Institute of Science and Technology Brugen af biomasseafledt
Den højeste varmebestandige plast nogensinde er udviklet af biomasseFigur 1. Udviklingsstrategi for cellulose-afledt PBI og PBI/PA film med ultrahøj termomodstand og rammehæmning. Kredit:Japan Advanced Institute of Science and Technology Brugen af biomasseafledt -
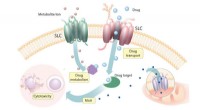 Afdækning af nye forhold mellem SLC'er og cytotoksiske lægemidler i humane cellerSolute Carriers (SLCer) påvirker optagelsen, metabolisme og virkningsmekanisme (MoA) af cytotoksiske lægemidler. Kredit:© Enrico Girardi / CeMM CeMM Forskere har undersøgt, hvordan solute carriers
Afdækning af nye forhold mellem SLC'er og cytotoksiske lægemidler i humane cellerSolute Carriers (SLCer) påvirker optagelsen, metabolisme og virkningsmekanisme (MoA) af cytotoksiske lægemidler. Kredit:© Enrico Girardi / CeMM CeMM Forskere har undersøgt, hvordan solute carriers -
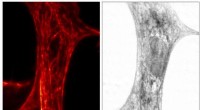 Kombineret røntgen- og fluorescensmikroskop afslører usete molekylære detaljerSTED-billede (venstre) og røntgenbillede (højre) af den samme hjertevævscelle fra en rotte. For STED, netværket af actin filamenter i cellen, hvilket er vigtigt for cellens mekaniske egenskaber, er bl
Kombineret røntgen- og fluorescensmikroskop afslører usete molekylære detaljerSTED-billede (venstre) og røntgenbillede (højre) af den samme hjertevævscelle fra en rotte. For STED, netværket af actin filamenter i cellen, hvilket er vigtigt for cellens mekaniske egenskaber, er bl
- Kulstofregnskab skal indeholde bygrønt, siger forskere
- Effektivt materiale udviklet til at forhindre post-kirurgisk vedhæftning
- Sådan beregner du kølemængder
- Når de bliver ramt med et skarpt slag, har ioniske forbindelser tendens til hvad, mens metalliske s…
- Sammenlign klimaet i dag med det i en istid?
- Forskere lærer, hvordan hestegræs trækker fra sig herbicid


