Hvis to kloratomer skulle tiltrække elektroner fra calcium, ville de blive ladet.?
* calcium (CA) er et metal og har en tendens til at miste elektroner for at opnå en stabil elektronkonfiguration. Det har 2 valenselektroner (elektroner i dets yderste skal).
* klor (Cl) er en ikke -metal og har en tendens til at få elektroner for at opnå en stabil elektronkonfiguration. Det har 7 valenselektroner.
Når calcium og klor reagerer, får hvert kloratom et elektron fra calciumatomet. Dette efterlader calciumatomet med et +2 ladning og hvert kloratom med en -1 ladning.
Her er sammenbruddet:
* calcium: Ca → Ca²⁺ + 2e⁻ (mister 2 elektroner, bliver positivt ladet)
* klor: 2Cl + 2e⁻ → 2Cl⁻ (får 2 elektroner, hver bliver negativt ladet)
Resultatet er dannelsen af calciumchlorid (CACL₂), en ionisk forbindelse med en neutral samlet ladning.
 Varme artikler
Varme artikler
-
 Solbrint:Bedre fotoelektroder gennem flashopvarmningPulserende laseraflejring:En intens laserimpuls rammer et mål, der indeholder materialet, og transformerer det til et plasma, som derefter afsættes som en tynd film på et substrat. Kredit:R. Gottesman
Solbrint:Bedre fotoelektroder gennem flashopvarmningPulserende laseraflejring:En intens laserimpuls rammer et mål, der indeholder materialet, og transformerer det til et plasma, som derefter afsættes som en tynd film på et substrat. Kredit:R. Gottesman -
 Glow-in-the-mørke papir som en hurtig test for infektionssygdommeDenne papirstrimmel (ekstremt zoomet ind) indeholder to kopier af testen. De tre lysende prikker pr. test indikerer, at du kan kontrollere tre forskellige antistoffer inden for en test. Kredit:Bart va
Glow-in-the-mørke papir som en hurtig test for infektionssygdommeDenne papirstrimmel (ekstremt zoomet ind) indeholder to kopier af testen. De tre lysende prikker pr. test indikerer, at du kan kontrollere tre forskellige antistoffer inden for en test. Kredit:Bart va -
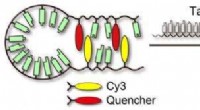 Cyaninfarvestoffer kunne forbedre effektiviteten af molekylære proberRNA-detektionsskema:Det hårnåleformede molekyle åbner sig hurtigt, kombineres med dets komplementære mål og fluorescerer klart. Kredit:Videnskab og teknologi for avancerede materialer Forskere bru
Cyaninfarvestoffer kunne forbedre effektiviteten af molekylære proberRNA-detektionsskema:Det hårnåleformede molekyle åbner sig hurtigt, kombineres med dets komplementære mål og fluorescerer klart. Kredit:Videnskab og teknologi for avancerede materialer Forskere bru -
 Skorpiongift til at transportere stoffer ind i hjernenKæmpe gul israelsk skorpion. Kredit:Ester Inbar Peptider- og proteinlaboratoriet ved Institut for Forskning i Biomedicin (IRB Barcelona) har udgivet en artikel i Kemisk kommunikation beskriver b
Skorpiongift til at transportere stoffer ind i hjernenKæmpe gul israelsk skorpion. Kredit:Ester Inbar Peptider- og proteinlaboratoriet ved Institut for Forskning i Biomedicin (IRB Barcelona) har udgivet en artikel i Kemisk kommunikation beskriver b
- Sorter delene af en nukleinsyre afhængigt af om hver forekommer udelukkende i DNA RNA eller begge t…
- Briter og tyskere har meget forskellige syn på fremtidens folkepensioner
- Storme fyldte 37 procent af CAs sne-vandsunderskud
- Som vil dissociere, når den placeres i vand a. CH3OH b. HCl c. KBr d. HClO4?
- Autonome svævefly kan flyve som en albatros, krydstogt som en sejlbåd
- Indias Infosys rapporterer en stigning i overskuddet på 3,7 procent, savner estimater


