Hvorfor stiger opløseligheden af jod i vand, når koncentration af kaliumiodid øges?
Her er en sammenbrud:
1. jod i vand: Jod (i 2 ) er kun lidt opløselig i vand. Dette skyldes, at jod er et ikke -polært molekyle, og vand er et polært opløsningsmiddel. Samspillet mellem dem er svag.
2. kaliumiodid: Kaliumiodid (KI) er opløseligt i vand, der adskiller sig i kaliumioner (K + ) og iodidioner (i - ).
3. triiodidiondannelse: Når jod tilsættes til en opløsning, der indeholder iodidioner, opstår der en reaktion:
`` `
Jeg 2 (aq) + i - (aq) ⇌ i 3 - (aq)
`` `
Triiodidionen (i 3 - ) dannes, som er opløselig i vand.
4. le Chateliers princip: Dannelsen af triiodidioner er en ligevægtsreaktion. Forøgelse af koncentrationen af iodidioner (ved at tilføje flere Ki) skifter ligevægt til højre, hvilket favoriserer dannelsen af flere triiodidioner.
5. Øget opløselighed: Efterhånden som flere triiodidioner dannes, "opløses" mere jod "i opløsningen, hvilket fører til en stigning i den samlede opløselighed af jod.
Kortfattet: Tilstedeværelsen af iodidioner fra kaliumiodid fremmer dannelsen af opløselige triiodidioner, hvilket effektivt øger opløseligheden af jod i vand.
 Varme artikler
Varme artikler
-
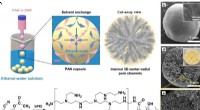 Ny teknologi øger dramatisk genindvindingsgraden af ædle metaller fra affaldFremstillingsprocessen og de fysiske/kemiske strukturer af guldgenvindingsmateriale. Kredit:Korea Institute of Science and Technology (KIST) I Sydkorea, som er afhængig af import for 99,3 % af sine
Ny teknologi øger dramatisk genindvindingsgraden af ædle metaller fra affaldFremstillingsprocessen og de fysiske/kemiske strukturer af guldgenvindingsmateriale. Kredit:Korea Institute of Science and Technology (KIST) I Sydkorea, som er afhængig af import for 99,3 % af sine -
 Ved at kopiere bakterielle enzymer, laboratoriet lærer hurtigt at syntetisere ny klasse af antibiot…Jordbakterien Pseudomonas fluorescens, her lyser stærkt under ultraviolet lys, udstråler et antibiotikum kaldet obafluorin, der har en ny ß-lactonstruktur. Kredit:Washington University i St. Louis
Ved at kopiere bakterielle enzymer, laboratoriet lærer hurtigt at syntetisere ny klasse af antibiot…Jordbakterien Pseudomonas fluorescens, her lyser stærkt under ultraviolet lys, udstråler et antibiotikum kaldet obafluorin, der har en ny ß-lactonstruktur. Kredit:Washington University i St. Louis -
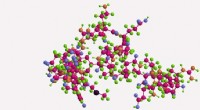 En lovende strategi til at øge aktiviteten i antimikrobielle peptiderKredit:Institut national de la recherche scientifique I en artikel offentliggjort for nylig i Plos One , forskere fra INRS-Institut Armand-Frappier Research Center rapporterede en strategi, der
En lovende strategi til at øge aktiviteten i antimikrobielle peptiderKredit:Institut national de la recherche scientifique I en artikel offentliggjort for nylig i Plos One , forskere fra INRS-Institut Armand-Frappier Research Center rapporterede en strategi, der -
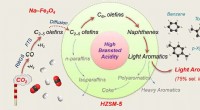 Forskere syntetiserer lette aromater fra kuldioxidhydrogeneringNøjagtig regulering af Brønsted -syresider for at fremme syntesen af lette aromater via CO2 -hydrogenering. Kredit:WEI Jian og YAO Ruwei Aromater produceres normalt fra råolie via kemiske omdann
Forskere syntetiserer lette aromater fra kuldioxidhydrogeneringNøjagtig regulering af Brønsted -syresider for at fremme syntesen af lette aromater via CO2 -hydrogenering. Kredit:WEI Jian og YAO Ruwei Aromater produceres normalt fra råolie via kemiske omdann
- Hvad mener du med metaaluminat?
- Lyser på de skjulte egenskaber ved kvantematerialer
- Mod en miljøvenlig produktion af aktive farmaceutiske ingredienser med en flowreaktor
- Hvilke celler proces forekommer i mitokondrierne?
- Hvor meget ATP produceres, hvis der ikke er ilt?
- Analyse af luftstrømme udsendt af kunstnere fra MET fremhæver COVID-19-risici


