Ved at kopiere bakterielle enzymer, laboratoriet lærer hurtigt at syntetisere ny klasse af antibiotiske molekyler rent, effektivt
Jordbakterien Pseudomonas fluorescens, her lyser stærkt under ultraviolet lys, udstråler et antibiotikum kaldet obafluorin, der har en ny ß-lactonstruktur. Kredit:Washington University i St. Louis
Den aktive komponent i vidundermedicinet penicillin og beslægtede antibiotika, såsom cephalosporiner, er en "fortryllet ring, "kaldet β-lactam-ringen. Antibiotika, der inkluderer disse ringe, er uden tvivl de vigtigste lægemidler i menneskets historie, på egen hånd øget den globale levealder med anslået fem år.
"Folk siger ofte, at vi er ved at løbe tør for antibiotika, men der er mere end 20, 000 molekyler med antibiotisk aktivitet i Handbook of Antibiotics, "sagde Timothy Wencewicz, en kemiker ved Washington University i St. Louis, der har specialiseret sig i design af antibiotika.
"Færre end 1 procent af dem er nogensinde blevet betragtet som en potentiel klinisk kandidat. De svinder, fordi det tager så meget tid og omhu at forberede et molekyle til brug som et lægemiddel.
Wencewicz valgte omhyggeligt et af disse molekyler, obafluorin, til videre undersøgelse. Oblafluorin, opdaget i 1984 af Squibb Institute, fremstilles af en fluorescerende stamme af jordbakterier, der danner biofilm på planterødder.
Ligesom penicillin, obafluorin har en fireleddet ring. En fireleddet ring belaster de bindingsvinkler, som carbon foretrækker at anvende, forklarer Wencewicz. "Stammen gør disse ringe til molekylære bomber, der går af, når de sættes på det rigtige sted på det rigtige tidspunkt, som er nyttig til at dræbe mikrober, " han sagde.
Men fordi en fireledsring er ustabil, disse molekyler er også korte og svære at lave. Det tog år for kemikere at lære at syntetisere penicillin fra kemikalier og derefter finde ud af, hvordan svampe gør det. Antibiotikummet fremstilles stadig ved at fermentere en penicillinudstrømmende svampestamme i kæmpe rustfrit stålkar.
Wencewicz -laboratoriet var i stand til at springe hele processen, ved at bruge genetik til at nulstille det biosyntetiske maskineri, som bakterier bruger til at fremstille obafluorin og derefter til at rekonstruere det flertrins, enzymkatalyseret proces i laboratoriet.

Betalactamringen kobler tre carbonatomer og et nitrogen, der henviser til, at beta-lactonringen består af tre carbonatomer og et oxygen. "De er i det væsentlige iso-elektron; de ser og lugter det samme, "Wencewicz sagde." Men ilt er forskelligt fra nitrogen, og så har de en anden palet af bioaktiviteter og hæmmer et andet sæt målenzymer. "Kredit:Wencewicz
Wencewicz, kandidatstuderende Mars Reck og Jason Schaffer, og bachelor Neha Prasad beskriver det komplette biosyntetiske maskineri til samling af ß-lacton-obafluorin i 15. maj-udgaven af Naturens kemiske biologi .
Ss-lactonerne hæmmer en stor klasse enzymer kaldet serinhydrolaser. "Der er hundredvis af kendte serinhydrolaser, og de er impliceret i mange menneskelige sygdomme, "Sagde Wencewicz. Ss-lactonerne kan vise sig nyttige i behandlingen af kræft og fedme, samt smitsomme sygdomme.
En mørk vej bragt frem i lyset
Obafluorin er et peptid, en kort kæde af forbundne aminosyrer. De fleste peptider produceres af en cellulær maskine kaldet ribosomet, som fremstiller en række forskellige peptider. Obafluorin, imidlertid, samles ikke af ribosomet, men af ikke-ribosomalt peptidsyntetase (NRPS), et flerdelt enzym, der kun syntetiserer én type peptid.
Ribosomerne gør de lange peptider kaldet proteiner, der er afgørende for livet, Sagde Wencewicz. Ribosomer har udviklet sig over millioner af år til at være utrolig effektive og præcise, han tilføjede, men de bruger et begrænset sæt af aminosyre byggesten.
Antibiotika og andre sekundære metabolitter, der er nyttige, men ikke afgørende for livet, samles mere eller mindre efter behov af NRPS samlebånd. Disse NRPS'er er i stand til at forbinde tusinder af forskellige aminosyre byggesten til dannelse af strukturelt forskellige små peptider med vigtig biologisk aktivitet.
NRPS'er er i det væsentlige en række enzymer, der er slået sammen til et stort protein med mange domæner, som hver udfører et trin i peptidsamling. "De er snarere som Henry Ford samlebånd, "Sagde Wencewicz.
Wencewicz -laboratoriet identificerede genklyngen i Pseudomonas fluorescerende, der gør NRPS og lavede de fem enzymer, generne koder.
Det femte enzym viste sig at være særligt interessant. Det er en usædvanlig thioesterase, der er ansvarlig for ß-lactonringdannelse, når peptidet frigives fra NRPS. I modsætning til andre thioesteraseenzymer, obafluorintioesterasen indbefatter en sjælden katalytisk aminosyre, der genererer et reaktivt thioester -mellemprodukt. Denne usædvanlige kemi gør det muligt for NRPS at overvinde energibarrieren, der ellers forhindrer dannelsen af en anstrengt ring.
Mange flere ringe kommer
"Vi har nu en komplet enzymatisk platform til fremstilling af ß-lactonpeptider af enkle udgangsmaterialer, "Wencewicz sagde." Da vi kender de gensekvenser, der koder for denne samlebånd, vi bruger magten i moderne genom-sekventering til at søge efter og lave nye ß-lactoner fremstillet af andre organismer. "
Enhver, der kender den lange og frustrerende kamp om at producere nok penicillin til at hjælpe sårede soldater under Anden Verdenskrig, kan kun undre sig over de betagende fremskridt inden for genetik og kemi, der har gjort det muligt for Wencewicz -laboratoriet at kollapse arbejdet i mange årtier på få år.
 Varme artikler
Varme artikler
-
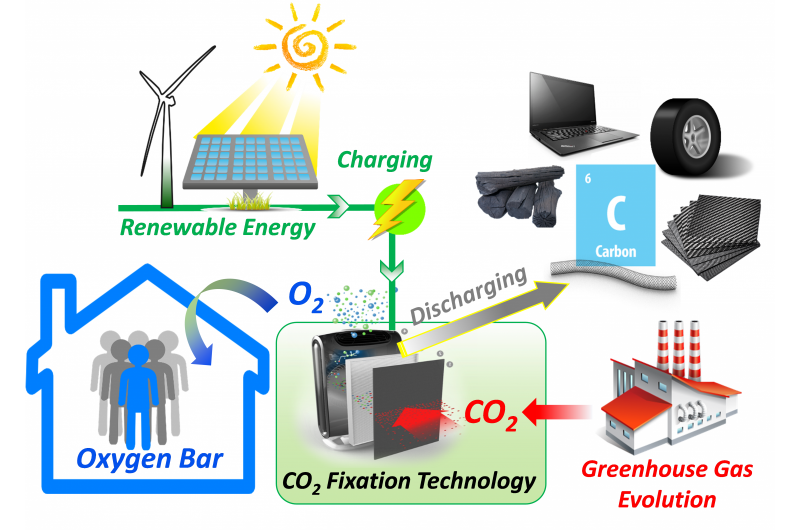 En batteri-inspireret strategi for carbonfikseringEt flowchart over energilagring og kulstoffiksering ved hjælp af Li-CO2-teknologi. Kredit:Qiao et al. Forskere, der arbejder hen imod det undvigende lithium-luftbatteri, opdagede en uventet tilgan
En batteri-inspireret strategi for carbonfikseringEt flowchart over energilagring og kulstoffiksering ved hjælp af Li-CO2-teknologi. Kredit:Qiao et al. Forskere, der arbejder hen imod det undvigende lithium-luftbatteri, opdagede en uventet tilgan -
 Dampanalyse i realtid kan forbedre træning af hunde, der registrerer eksplosive stofferKredit:American Chemical Society Med en lugtesans meget større end mennesker, hunde betragtes som guldstandarden for eksplosiv detektion i mange situationer. Men det betyder ikke, at der ikke er p
Dampanalyse i realtid kan forbedre træning af hunde, der registrerer eksplosive stofferKredit:American Chemical Society Med en lugtesans meget større end mennesker, hunde betragtes som guldstandarden for eksplosiv detektion i mange situationer. Men det betyder ikke, at der ikke er p -
 Første luminescerende molekylære system med en lavere kritisk opløsningstemperaturFigur 1:Billeder af LCST-system under UV-lysbestråling ved lav temperatur (venstre), høj temperatur (i midten), og i løbet af faldende temperatur (højre). Kredit:Osaka University Afhængig af deres
Første luminescerende molekylære system med en lavere kritisk opløsningstemperaturFigur 1:Billeder af LCST-system under UV-lysbestråling ved lav temperatur (venstre), høj temperatur (i midten), og i løbet af faldende temperatur (højre). Kredit:Osaka University Afhængig af deres -
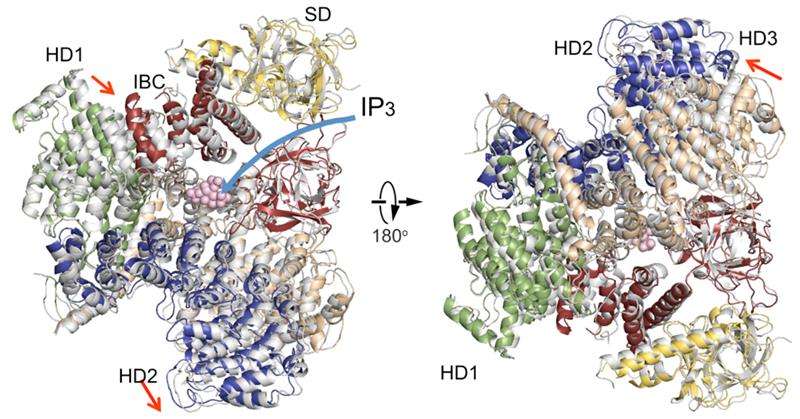 Atomstruktur afslører, hvordan celler oversætter miljøsignalerEn sammenligning af IP3R cytosoliske domænestrukturer i fravær af IP3 (farvet) med en i nærvær af IP3 (grå). Domæneorganisation. Undertrykkerdomæne (SD), gul; IP3-bindende kerne (IBC), rød; spiralform
Atomstruktur afslører, hvordan celler oversætter miljøsignalerEn sammenligning af IP3R cytosoliske domænestrukturer i fravær af IP3 (farvet) med en i nærvær af IP3 (grå). Domæneorganisation. Undertrykkerdomæne (SD), gul; IP3-bindende kerne (IBC), rød; spiralform
- En ny rejse ind i Jorden for at udforske rummet
- Private virksomheder lancerer et nyt rumkapløb - her er hvad de kan forvente
- Udseendet af dybhavsfisk signalerer ikke kommende jordskælv i Japan
- Stor udendørs undersøgelse viser, at biodiversitet forbedrer stabiliteten af algebiobrændstofsy…
- Små guldkugler kan manipuleres på overflader ved hjælp af fordampning af opløsningsmiddel
- Succes handler om at skabe sociale forbindelser - eller er det?


