Hvor mange elektroner vil fluorandel for at få kovalente bindinger til at afslutte sit yderste energiniveau?
Her er hvorfor:
* fluorens elektronkonfiguration: Fluor har 9 elektroner med konfigurationen 2, 7. Dette betyder, at den har 7 elektroner i sin yderste skal (Valence Shell).
* octet regel: Atomer har en tendens til at vinde, miste eller dele elektroner for at opnå en stabil konfiguration af 8 elektroner i deres valensskal (Octet -regel).
* Deling for stabilitet: Fluor har brug for endnu en elektron for at nå en fuld oktet. Det opnår dette ved at dele et elektron med et andet atom og danne en enkelt kovalent binding.
Fortæl mig, hvis du gerne vil udforske andre eksempler på kovalent binding!
 Varme artikler
Varme artikler
-
 Nye mål i kampen mod antibiotikaresistensProfessor Stephan A. Sieber og Dr. Sabine Schneider i laboratoriet for formanden for organisk kemi II ved det tekniske universitet i München. Kredit:Andreas Battenberg / TUM Bakterier er i stigend
Nye mål i kampen mod antibiotikaresistensProfessor Stephan A. Sieber og Dr. Sabine Schneider i laboratoriet for formanden for organisk kemi II ved det tekniske universitet i München. Kredit:Andreas Battenberg / TUM Bakterier er i stigend -
 Opsnuse forfalskede spiritusEn bærbar enhed med en avanceret sensor kan opsnuse forfalskede spiritus. Kredit:Kenneth S. Suslick, Ph.D. Udvandet eller falsk spiritus kan høste økonomiske belønninger for ondsindede personer, m
Opsnuse forfalskede spiritusEn bærbar enhed med en avanceret sensor kan opsnuse forfalskede spiritus. Kredit:Kenneth S. Suslick, Ph.D. Udvandet eller falsk spiritus kan høste økonomiske belønninger for ondsindede personer, m -
 Effektiv, stabilt termoelektrisk modul baseret på højtydende væskelignende materialerKredit:CC0 Public Domain Baseret på højtydende væskelignende materialer, videnskabsmænd fra Shanghai Institute of Ceramics ved det kinesiske videnskabsakademi og Northwestern University i USA frem
Effektiv, stabilt termoelektrisk modul baseret på højtydende væskelignende materialerKredit:CC0 Public Domain Baseret på højtydende væskelignende materialer, videnskabsmænd fra Shanghai Institute of Ceramics ved det kinesiske videnskabsakademi og Northwestern University i USA frem -
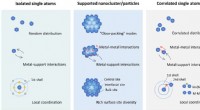 Nye elektrokatalysatorer varsler kulstofneutralitetC-SACer med metal-metal interaktioner. Sammenligning af C-SACer med de konventionelle isolerede SACer og understøttede metalliske klynge/nanopartikelkatalysatorer fra perspektivet af rumlig fordeling,
Nye elektrokatalysatorer varsler kulstofneutralitetC-SACer med metal-metal interaktioner. Sammenligning af C-SACer med de konventionelle isolerede SACer og understøttede metalliske klynge/nanopartikelkatalysatorer fra perspektivet af rumlig fordeling,
- Forskere opfinder en ny følende øjenmaske
- Hvor mange planeter er der ikke dværgplaneter?
- Hvorfor hverken væsker eller gasser har faste former?
- Amazon afgør løntvist med WGA om rester for forfattere
- Plastik fra træ? Røntgenanalyse viser vej til ligninbaserede komponenter fremstillet efter mål
- Hvor kommer det meste af ilten i atmosfæren fra?


