Hvad er den termiske nedbrydning af natriumcarbonat?
Her er hvorfor:
* stærke ioniske bindinger: Natriumcarbonat er en ionisk forbindelse med stærke elektrostatiske interaktioner mellem natriumkationer (Na⁺) og carbonatanioner (co₃²⁻). Disse obligationer kræver en betydelig mængde energi for at bryde.
* Høj nedbrydningstemperatur: Nedbrydningen af natriumcarbonat ville kræve temperaturer meget højere end dets smeltepunkt (851 ° C). Under sådanne ekstreme forhold kan carbonatanionen muligvis nedbrydes i kuldioxid og oxidioner, men dette er ikke en typisk termisk nedbrydningsproces.
I stedet for termisk nedbrydning kan natriumcarbonat gennemgå reaktioner med syrer:
* Når det opvarmes med stærke syrer som saltsyre (HCI), frigiver natriumcarbonat kuldioxidgas, vand og danner natriumchlorid (NaCl):
Na₂co₃ (S) + 2HCI (aq) → 2naCl (aq) + h₂o (l) + co₂ (g)
I resuméet Natriumcarbonat er en stabil forbindelse og nedbrydes ikke let ved opvarmning. I stedet reagerer det med syrer for at producere kuldioxid og andre produkter.
Sidste artikelEr ammoniak NH3 organisk eller uorganisk?
Næste artikelHvad er den primære og sekundære funktion af flaske?
 Varme artikler
Varme artikler
-
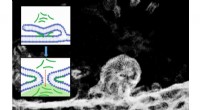 Hvordan trænger peptider ind i celler? To sider af samme møntElektronmikroskopibillede af en todelt cellemembran og det tilsvarende molekylære skema for processen. Kredit:@ IOCB Prag Den simple transport af lægemidler direkte ind i cellerne er et af de prim
Hvordan trænger peptider ind i celler? To sider af samme møntElektronmikroskopibillede af en todelt cellemembran og det tilsvarende molekylære skema for processen. Kredit:@ IOCB Prag Den simple transport af lægemidler direkte ind i cellerne er et af de prim -
 Gør emballagematerialer genanvendeligeTegneserie lavet af Jiaying Li Hvis det er op til UT-Ph.D. studerende Jiaying Li, vi vil ikke længere have et sølv lag i madpakker som chipsposer. I hendes seneste publikation, hun beskriver en fo
Gør emballagematerialer genanvendeligeTegneserie lavet af Jiaying Li Hvis det er op til UT-Ph.D. studerende Jiaying Li, vi vil ikke længere have et sølv lag i madpakker som chipsposer. I hendes seneste publikation, hun beskriver en fo -
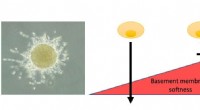 Ny opdagelse kan muliggøre præcis forudsigelse af kræftspredning, før kræft udvikler sigVENSTRE:Spheroid af brystkræftceller, der bryder gennem basalmembranen for at invadere i det omkringliggende område. Denne evne bestemmes af forholdet mellem netrin-molekyler til stede i basalmembrans
Ny opdagelse kan muliggøre præcis forudsigelse af kræftspredning, før kræft udvikler sigVENSTRE:Spheroid af brystkræftceller, der bryder gennem basalmembranen for at invadere i det omkringliggende område. Denne evne bestemmes af forholdet mellem netrin-molekyler til stede i basalmembrans -
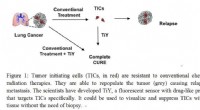 Alsidig sensor mod tumorinitierende cellerDe fleste kræftdødsfald skyldes tilbagevendende eller metastatiske tumorer. Konventionelle terapier er målrettet mod hurtigt delende tumorceller, men er ude af stand til at udrydde de stærkt kemoresis
Alsidig sensor mod tumorinitierende cellerDe fleste kræftdødsfald skyldes tilbagevendende eller metastatiske tumorer. Konventionelle terapier er målrettet mod hurtigt delende tumorceller, men er ude af stand til at udrydde de stærkt kemoresis
- Meget effektiv og stabil nær-infrarød fosfor til nattesyn og bio-billeddannelse
- Undersøgelse udvider, hvad vi ved om naturlige, billige måder at fjerne forurenende stoffer fra va…
- Hvordan påvirker eddike stål?
- Sjældne jordarters grundstoffer opdaget i Georgia kaolinminer, undersøgelse finder
- Forskere kæmper mod udryddelse for at afsløre træers kræftbekæmpende egenskaber
- Forskerhold udvikler et nyt system til at spore hjernekemikalier


