Hvad sker der, når du blander fosfor med andre elementer?
med metaller:
* fosfider: Fosfor kombineres med mange metaller til dannelse af phosphider. Disse forbindelser har en bred vifte af egenskaber, fra den meget reaktive til den relativt inerte.
* Eksempler: Aluminiumphosphid (ALP), der bruges som fumigant; Calciumphosphid (CA3P2), der bruges til generering af phosphinas; Natriumphosphid (Na3p), en meget reaktiv forbindelse anvendt i kemisk syntese.
* metalphosphides: Disse er generelt ikke-metalliske, sprøde faste stoffer med forskellige ledningsgrader.
med ikke-metaler:
* Oxider: Fosfor danner forskellige oxider, herunder:
* fosfor trioxid (P4O6): Et hvidt, krystallinsk fast stof, der let reagerer med vand til dannelse af fosforsyre.
* phosphor pentoxid (P4O10): Et meget reaktivt, deliquescent hvidt pulver anvendt som tørringsmiddel og i produktionen af fosforsyre.
* halogenider: Fosfor danner trihalider (PX3) og pentahalider (PX5) med halogener som chlor, brom og jod.
* Eksempler: Phosphor -trichlorid (PCL3), anvendt som reagens i organisk syntese; Phosphor pentachlorid (PCL5), anvendt til produktion af andre fosforforbindelser.
* sulfider: Fosfor kan danne sulfider som fosfor pentasulfid (P4S10) og fosfortrisulfid (P4S3).
* phosphor pentasulfid (P4S10): Anvendt til produktion af pesticider og i syntesen af andre svovlholdige forbindelser.
* nitrogen: Fosfor kan danne forbindelser med nitrogen, herunder:
* fosfornitrid (P3N5): Et hvidt, ildfast fast stof, der bruges til produktion af keramik med høj temperatur.
med organiske forbindelser:
* organophosphorforbindelser: Fosfor danner en lang række organiske forbindelser, som er vigtige i mange områder, herunder:
* fosfater: Uorganiske fosfater (PO43-) er essentielle for livet, der findes i DNA, RNA og ATP.
* fosfiner: Organofosfiner anvendes i katalyse som ligander i koordinationskemi og som mellemprodukter i syntesen af andre organophosphorforbindelser.
* fosfonater: Brugt i pesticider, flammehæmmere og som tilsætningsstoffer i plast.
* fosfater estere: Brugt i vaskemidler, blødgører og som flammehæmmere.
nøgle ting at huske:
* reaktivitet: Fosfor kan være meget reaktiv, især i sin hvide form. Dette skyldes dens lille størrelse og tilstedeværelsen af uparrede elektroner.
* Forskellige former: Fosfor findes i forskellige allotroper, herunder hvid, rød og sort fosfor, hver med unikke egenskaber.
* Betydning: Fosforforbindelser er afgørende i mange områder, herunder landbrug, industri og medicin.
Bemærk, at blanding af fosfor med andre elementer kan være farlige, og der skal altid tages passende sikkerhedsforholdsregler.
Sidste artikelHvilket element har lignende kemiske egenskaber som nitrogen?
Næste artikelHvad er den polyatomiske forbindelse i RB PO4-3?
 Varme artikler
Varme artikler
-
 Letvægts elektriske armbåndsvarmere til konstant, bærbar varmeEt elektrisk ledende og holdbart garn blev syet på stof og blev en bærbar varmelegeme (høje temperaturer angivet med gule og røde), når der blev påført en sikker spænding. Kredit:American Chemical Soc
Letvægts elektriske armbåndsvarmere til konstant, bærbar varmeEt elektrisk ledende og holdbart garn blev syet på stof og blev en bærbar varmelegeme (høje temperaturer angivet med gule og røde), når der blev påført en sikker spænding. Kredit:American Chemical Soc -
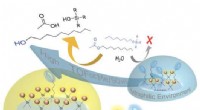 Nøglebeviser, der forbinder hydrofobicitet med effektiv syrekatalyseForenklet skematisk, der viser, hvordan alkylacetater med lange haler ikke kan nærme sig sure sulfo-steder (blå skiver) i hydrofile miljøer; imidlertid, de kan nærme sig hydrofobe miljøer med flere me
Nøglebeviser, der forbinder hydrofobicitet med effektiv syrekatalyseForenklet skematisk, der viser, hvordan alkylacetater med lange haler ikke kan nærme sig sure sulfo-steder (blå skiver) i hydrofile miljøer; imidlertid, de kan nærme sig hydrofobe miljøer med flere me -
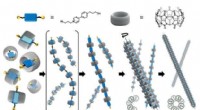 Selvsamlet kunstig mikrotubuli som LEGO byggeklodserHierarkisk selvsamling af polypseudorotaxaner til kunstige mikrotubuli. Kredit:Kimoon Kim (POSTECH) Simple LEGO klodser kan samles til mere komplicerede strukturer, som yderligere kan associeres t
Selvsamlet kunstig mikrotubuli som LEGO byggeklodserHierarkisk selvsamling af polypseudorotaxaner til kunstige mikrotubuli. Kredit:Kimoon Kim (POSTECH) Simple LEGO klodser kan samles til mere komplicerede strukturer, som yderligere kan associeres t -
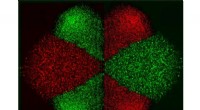 Forskere udvikler mikro-elektro-fluidisk probe (MeFP) til at isolere og mønstre cellerEt dynamisk mønster af forskellige celletyper isoleret og deponeret ved hjælp af den udviklede Micro-electro-fluidic Probe (MeFP). Kredit:NYU Abu Dhabi fakultet Mohammad Qasaimeh Et team af forske
Forskere udvikler mikro-elektro-fluidisk probe (MeFP) til at isolere og mønstre cellerEt dynamisk mønster af forskellige celletyper isoleret og deponeret ved hjælp af den udviklede Micro-electro-fluidic Probe (MeFP). Kredit:NYU Abu Dhabi fakultet Mohammad Qasaimeh Et team af forske
- Hvilke gener er ikke en del af LAC -operonet?
- Sådan får du 12 volt fra en 48 Volt Golf Cart
- Jagten på bæredygtige læderalternativer
- Hvad Darwin ikke kunne se:Ekspedition for at afsløre usynligt liv på Galápagos
- Datalagring ved hjælp af individuelle molekyler
- NASA finder Nardas-rester, der bringer regn til Mexico, på vej til det sydvestlige USA


