Hvilket element har lignende kemiske egenskaber som nitrogen?
Her er hvorfor:
* de er begge i gruppe 15 (VA) i den periodiske tabel. Dette betyder, at de har det samme antal valenselektroner (5), som er de elektroner, der er involveret i kemisk binding.
* Lignende elektronegativitet: Både nitrogen og fosfor har relativt høje elektronegativitetsværdier, hvilket betyder, at de har en tendens til at tiltrække elektroner i kemiske bindinger.
* Evne til at danne flere obligationer: Begge elementer kan danne enkelt-, dobbelt- og tredobbeltbindinger med andre elementer.
* Dannelse af hydrider: De danner hydrider (forbindelser med brint) med lignende egenskaber. For eksempel er ammoniak (NH3) og phosphin (PH3) begge gasser ved stuetemperatur.
Der er dog også nogle forskelle mellem nitrogen og fosfor:
* nitrogen er mere elektronegativ end fosfor.
* fosfor kan danne mere komplekse forbindelser end nitrogen.
* fosfor findes i flere allotropiske former (forskellige strukturelle former), mens nitrogen kun har en.
Generelt deler nitrogen og fosfor mange ligheder på grund af deres lignende elektroniske konfigurationer og positioner i den periodiske tabel, hvilket fører til lignende kemiske egenskaber.
 Varme artikler
Varme artikler
-
 Ny teknik muliggør 3D-print med pasta af silikonepartikler i vandNy teknik udgivet i Avancerede materialer viser processen med 3-D-print af silikonegummi. Kredit:Orlin Velev, NC State University Ved at bruge principperne bag dannelsen af sandslotte fra vådt
Ny teknik muliggør 3D-print med pasta af silikonepartikler i vandNy teknik udgivet i Avancerede materialer viser processen med 3-D-print af silikonegummi. Kredit:Orlin Velev, NC State University Ved at bruge principperne bag dannelsen af sandslotte fra vådt -
 Meget ensartet og lav hysterese tryksensor for at øge praktisk anvendelighedFigur 1. Billede af en porøs elastomerskabelon med ensartet porestørrelse og form (til venstre), Graf, der viser høj ensartethed i sensorernes ydeevne (højre). Kredit:Korea Advanced Institute of Scien
Meget ensartet og lav hysterese tryksensor for at øge praktisk anvendelighedFigur 1. Billede af en porøs elastomerskabelon med ensartet porestørrelse og form (til venstre), Graf, der viser høj ensartethed i sensorernes ydeevne (højre). Kredit:Korea Advanced Institute of Scien -
 Ny metode til at fjerne olie fra vandEn dråbe råolie på en vandoverflade adsorberes inden for få sekunder af et blad af den flydende bregne Salvinia og trækkes op af vandet. Kredit:W. Barthlott, M. Mail/Uni Bonn Olie udgør en betydel
Ny metode til at fjerne olie fra vandEn dråbe råolie på en vandoverflade adsorberes inden for få sekunder af et blad af den flydende bregne Salvinia og trækkes op af vandet. Kredit:W. Barthlott, M. Mail/Uni Bonn Olie udgør en betydel -
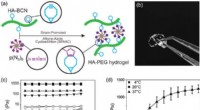 3-D dyrkning af hepatocytter på en lever-på-en-chip-enhed(a) Skematisk repræsentation af dannelsen af HA-PEG-hydrogeler gennem en stamme-promoveret alkyn-azid-cycloadditionsreaktion. (b) Fotografi af en HA-PEG hydrogel efter dannelse. (c) Frekvenssweep af
3-D dyrkning af hepatocytter på en lever-på-en-chip-enhed(a) Skematisk repræsentation af dannelsen af HA-PEG-hydrogeler gennem en stamme-promoveret alkyn-azid-cycloadditionsreaktion. (b) Fotografi af en HA-PEG hydrogel efter dannelse. (c) Frekvenssweep af
- Sentinel-1-satellitter bekræfter, at San Franciscos Millenium Tower er ved at synke
- The Scutoid:Hvordan vi opdager nye former
- Hvordan en dødelig landsvamp begyndte at dræbe havpattedyr i Salishhavet
- En reaktion på den visuelle klippe antages at måle hende?
- Er vores knogler veldesignede? Insekter og krabber har et ben på os
- Påvirker deltagelse i lotteriet forbrugernes selvkontrol?


