Hvad er forskel mellem kemisk termodynamisk og kinetik.?
Kemisk termodynamik
* fokus: Beskæftiger sig med de energiændringer, der forekommer under kemiske reaktioner, og betingelserne, under hvilke disse reaktioner er foretrukket eller ej.
* Nøglekoncepter:
* entalpi (ΔH): Varme absorberet eller frigivet under en reaktion.
* entropi (ΔS): Mål for et systems lidelse eller tilfældighed.
* gibbs fri energi (ΔG): Bestemmer spontaniteten (gennemførligheden) af en reaktion.
* ligevægtskonstant (K): Angiver de relative mængder af reaktanter og produkter i ligevægt.
* spørgsmål, det svarer:
* Er en reaktion spontan under givne betingelser?
* Hvor meget varme frigives eller absorberes under en reaktion?
* Hvad er ligevægtspositionen for en reaktion?
* Hvordan påvirker temperatur, tryk og koncentration ligevægten af en reaktion?
Kemisk kinetik
* fokus: Beskæftiger sig med hastighederne og mekanismerne for kemiske reaktioner.
* Nøglekoncepter:
* reaktionshastighed: Hvor hurtigt en reaktion fortsætter.
* rate lov: Matematisk ekspression, der relaterer hastigheden for en reaktion på koncentrationerne af reaktanter.
* Aktiveringsenergi (EA): Minimumsenergi kræves for at reaktanter skal danne produkter.
* reaktionsmekanisme: Trin-for-trin-proces, hvorved en reaktion opstår.
* spørgsmål, det svarer:
* Hvor hurtigt forekommer en reaktion?
* Hvilke faktorer påvirker reaktionshastigheden?
* Hvad er den mekanisme, hvormed en reaktion fortsætter?
* Hvordan kan vi kontrollere hastigheden for en reaktion?
analogi
Tænk på en biltur:
* termodynamik er som at vide, om du har nok gas til at nå din destination (spontanitet), og hvor meget gas du bruger (entalpi).
* kinetik er som at vide, hvor hurtigt du kommer dertil (hastighed), og hvilken rute du tager (mekanisme).
forhold
Selvom termodynamik og kinetik er separate felter, er de sammenflettet:
* termodynamik Kan forudsige, om en reaktion vil forekomme, men den fortæller dig ikke, hvor hurtigt det vil ske.
* kinetik Kan fortælle dig, hvor hurtigt en reaktion opstår, men den fortæller dig ikke, om reaktionen er spontan eller ej.
Eksempler:
* termodynamik: Forudsigelse af, om en reaktion vil frigive varme (eksotermisk) eller absorbere varme (endotermisk).
* kinetik: Bestemmelse af halveringstiden for en radioaktiv isotop (hvor lang tid det tager for halvdelen af isotopen at henfalde).
Kortfattet
Termodynamik og kinetik er begge vigtige for at forstå kemiske reaktioner. Termodynamik fortæller os, om en reaktion er mulig, og kinetik fortæller os, hvor hurtigt det vil ske.
Sidste artikelHvilke af udsagn om atomet blev bevist falsk af J.J Thompson?
Næste artikelNår en væske opvarmes og bliver til vanddampe?
 Varme artikler
Varme artikler
-
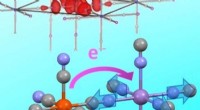 Ultrahurtig ladningsoverførsel i preussisk blå analogerKredit:Wiley Fotoinducerede ladningsoverførsler er en interessant elektronisk egenskab ved preussisk blå og nogle analogt strukturerede forbindelser. Et team af forskere har nu været i stand til a
Ultrahurtig ladningsoverførsel i preussisk blå analogerKredit:Wiley Fotoinducerede ladningsoverførsler er en interessant elektronisk egenskab ved preussisk blå og nogle analogt strukturerede forbindelser. Et team af forskere har nu været i stand til a -
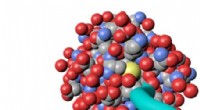 Miami kemis gennembrudsteknik muliggør design i grænsefladen mellem kemi og biologiEn syntetisk polymer (teal tube) konjugeret til et protein. Den lilla muffe på polymeren er en rapporteringsgruppe, nøglen til Konkolewicz og Pages teknik. Kredit:Miami University En teknik udvikl
Miami kemis gennembrudsteknik muliggør design i grænsefladen mellem kemi og biologiEn syntetisk polymer (teal tube) konjugeret til et protein. Den lilla muffe på polymeren er en rapporteringsgruppe, nøglen til Konkolewicz og Pages teknik. Kredit:Miami University En teknik udvikl -
 Knækker den katalytiske kodeKredit:Argonne National Laboratory Den nyudviklede evne til at udnytte tidligere utilgængelige skifergasforekomster i løbet af det sidste årti har skabt en rigelig kilde af gasser, herunder metan,
Knækker den katalytiske kodeKredit:Argonne National Laboratory Den nyudviklede evne til at udnytte tidligere utilgængelige skifergasforekomster i løbet af det sidste årti har skabt en rigelig kilde af gasser, herunder metan, -
 Bæredygtigt læder, garn og papir – fra brødspisende svampeSvampefibre kan omdannes til garn (venstre) eller en lædererstatning (højre). Kredit:Akram Zamani Din næste trendy håndtaske kunne være lavet af læder lavet af en svamp. I dag vil forskere beskrive
Bæredygtigt læder, garn og papir – fra brødspisende svampeSvampefibre kan omdannes til garn (venstre) eller en lædererstatning (højre). Kredit:Akram Zamani Din næste trendy håndtaske kunne være lavet af læder lavet af en svamp. I dag vil forskere beskrive
- En hurtig, en miljøvenlig måde at afise fly på
- Skaldyr, vilde eller opdrættede? Svaret kan være begge dele
- Hvad øger en planter evne til at absorbere vand og næringsstoffer?
- Hvilke kemiske strukturer og bindinger ville du forvente at finde i et umættet aromatisk carbonhydr…
- Hvad er Zen Stones?
- Kvanteeksperter gennemgår vigtige teknikker til at isolere Majoranas


