Hvor meget ville kogepunktet for vand stige, hvis 4 mol NaCI blev tilsat til 1 kg vand (kb =0,51 ° C/(mol/kg) for og i =2 NaCl)?
1. Beregn molaliteten af opløsningen:
* Molalitet (m) =mol opløst / kg opløsningsmiddel
* Molalitet =4 mol NaCl / 1 kg H₂O =4 mol / kg
2. Beregn kogepunkthøjden (ΔTB):
* ΔTb =kb * i * m
* ΔTB =0,51 ° C/(mol/kg) * 2 * 4 mol/kg =4,08 ° C
3. Beregn det nye kogepunkt:
* Det normale kogepunkt af vand er 100 ° C.
* Nyt kogepunkt =100 ° C + 4,08 ° C =104,08 ° C
Derfor ville kogepunktet for vand stige med 4,08 ° C til 104,08 ° C, når 4 mol NaCI tilsættes til 1 kg vand.
 Varme artikler
Varme artikler
-
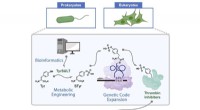 Fugleenzym peger mod nye terapierHvordan Rice University kemikere brugte en sjælden genetisk vej til metabolisk manipulation af celler, der fungerer som lægemiddelfabrikker til at lave thrombinhæmmere, der nedbryder blodpropper. Unde
Fugleenzym peger mod nye terapierHvordan Rice University kemikere brugte en sjælden genetisk vej til metabolisk manipulation af celler, der fungerer som lægemiddelfabrikker til at lave thrombinhæmmere, der nedbryder blodpropper. Unde -
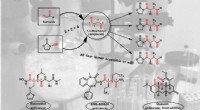 Når svovl forsvinder sporløstNy selektiv syntese af alle 1, 4-dicarbonylisomerer fra sulfoxider og udvalgte vigtige bioaktive forbindelser med 1, 4-dicarbonylmotiv. Kredit:© Maulide Group Mange naturprodukter og lægemidler ha
Når svovl forsvinder sporløstNy selektiv syntese af alle 1, 4-dicarbonylisomerer fra sulfoxider og udvalgte vigtige bioaktive forbindelser med 1, 4-dicarbonylmotiv. Kredit:© Maulide Group Mange naturprodukter og lægemidler ha -
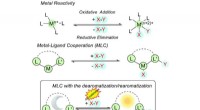 Forståelse af aromaticitet i katalyse for at låse op for nye mulighederFig. 1 Forskellige former for substrataktivering i konventionel og metal-ligand kooperativ katalyse. Kredit: Kemisk kommunikation (2021). DOI:10.1039/D1CC00528F Aromaticitet, et koncept, der norm
Forståelse af aromaticitet i katalyse for at låse op for nye mulighederFig. 1 Forskellige former for substrataktivering i konventionel og metal-ligand kooperativ katalyse. Kredit: Kemisk kommunikation (2021). DOI:10.1039/D1CC00528F Aromaticitet, et koncept, der norm -
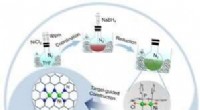 Forskere designer dinuclear-site katalysatorer og afslører den underliggende mekanismeSynteseskema. Kredit:DING Tao et al. Dinuclear-site katalysatorer (DSCer) har tiltrukket sig mere og mere opmærksomhed fra forskere på grund af deres fremragende katalytiske evne ved at inkorporer
Forskere designer dinuclear-site katalysatorer og afslører den underliggende mekanismeSynteseskema. Kredit:DING Tao et al. Dinuclear-site katalysatorer (DSCer) har tiltrukket sig mere og mere opmærksomhed fra forskere på grund af deres fremragende katalytiske evne ved at inkorporer
- John Deere 4400 Kombiner specifikationer
- Sammenlign og kontrast lagene sol med jord?
- Hvilken væske optages i fotosyntesen?
- Vi forventer, at byer fremmer multikulturalisme, men de kæmper
- Hvad kalder du noget andet metal end jern og legeringer?
- Forskere skaber kærlighedsmolekyle med færre komplikationer


