Hvordan skal du indikere, at der er flere polyatomiske ioner i en kemisk formel?
Sådan fungerer det:
1. Identificer den polyatomiske ion: En polyatomisk ion er en gruppe af atomer, der fungerer som en enkelt enhed med et ladning. Eksempler inkluderer:
* Sulfat (so₄²⁻)
* Nitrat (no₃⁻)
* Phosphate (Po₄³⁻)
2. vedhæng den polyatomiske ion i parenteser: Hvis du har brug for mere end en af de samme polyatomiske ion, skal du omslutte hele ionen i parentes.
3. placere et underskrift uden for parenteserne: Dette underskrift angiver antallet af tilstedeværende polyatomiske ioner.
Eksempel:
* Calciumphosphat: Formlen er CA₃ (PO₄) ₂. Dette indikerer tre calciumioner (Ca²⁺) og to fosfationer (Po₄³⁻).
Hvorfor parenteser er nødvendige:
* klarhed: Parenteser forhindrer forvirring over, hvilke elementer der er en del af den polyatomiske ion.
* Nøjagtighed: Brug af underskrifter direkte på elementerne inden for den polyatomiske ion ville ændre ionens kemiske sammensætning.
Lad mig vide, hvis du gerne vil have flere eksempler!
 Varme artikler
Varme artikler
-
 Materiale til ny generation atomreaktorer udvikletKredit:National University of Science and Technology MISIS Materialeforskere fra National University of Science and Technology MISIS (NUST MISIS) udviklede et unikt sandwich-stål-vanadium-stål mat
Materiale til ny generation atomreaktorer udvikletKredit:National University of Science and Technology MISIS Materialeforskere fra National University of Science and Technology MISIS (NUST MISIS) udviklede et unikt sandwich-stål-vanadium-stål mat -
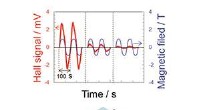 Daggry af organisk enkeltkrystal elektronikForskere ved Institute for Molecular Science, National Institutes of Natural Sciences (Japan) har udviklet en metode til højtydende doping af organisk enkeltkrystal. Desuden, det lykkedes dem at måle
Daggry af organisk enkeltkrystal elektronikForskere ved Institute for Molecular Science, National Institutes of Natural Sciences (Japan) har udviklet en metode til højtydende doping af organisk enkeltkrystal. Desuden, det lykkedes dem at måle -
 Ny proteinbilleddannelsesmetode baner vej for næste generations biomaterialer og vævsanalyseKredit:Unsplash/CC0 Public Domain Forskere har etableret en ny metode til billedproteiner, der kan føre til nye opdagelser i sygdomme gennem biologisk vævs- og celleanalyse og udvikling af nye bio
Ny proteinbilleddannelsesmetode baner vej for næste generations biomaterialer og vævsanalyseKredit:Unsplash/CC0 Public Domain Forskere har etableret en ny metode til billedproteiner, der kan føre til nye opdagelser i sygdomme gennem biologisk vævs- og celleanalyse og udvikling af nye bio -
 Video:Hvordan virker udløbsdatoer for lægemidlerKredit:The American Chemical Society Vi har alle set udløbsdatoerne på receptpligtig og håndkøbsmedicin. Hvad der er mindre indlysende for os som forbrugere, er, hvordan disse datoer bestemmes, o
Video:Hvordan virker udløbsdatoer for lægemidlerKredit:The American Chemical Society Vi har alle set udløbsdatoerne på receptpligtig og håndkøbsmedicin. Hvad der er mindre indlysende for os som forbrugere, er, hvordan disse datoer bestemmes, o
- Hvordan man beregner Dilutions
- Konsekvenserne af gletsjerskrumpning
- Sådan finder du linjer af Symmetry
- Når boliger rammer 40°C indeni, er det bedre at trække på beboernes lokale knowhow end at planlæ…
- Kvidring er velkommen hos fugle, men ikke i fusionsanordninger - forskere viser, at svag turbulens g…
- Hvilken form for stråling afgivet af jorden forårsager opvarmningsatmosfære?


