Foreslå hvorfor magnesiumchlorid kan fremstilles ved at blande med saltsyre, men kobber kan ikke syre?
Reaktivitetsserien
Nøglen er reaktivitetsserien af metaller. Denne serie rangerer metaller fra de fleste reaktive til mindst reaktive.
* magnesium (mg) er et mere reaktivt metal end kobber (CU) . Dette betyder, at magnesium har en større tendens til at miste elektroner og danne positive ioner.
Reaktionen med saltsyre
* Magnesium + saltsyre (HCI) → Magnesiumchlorid (MGCL₂) + brintgas (H₂)
I denne reaktion:
* Magnesium (Mg) reagerer med saltsyre (HCI) for at danne magnesiumchlorid (MGCL₂) og brintgas (H₂).
* Hydrogenionerne (H⁺) i syren reduceres til brintgas ved magnesium.
* Magnesium mister elektroner og danner magnesiumioner (mg²⁺), som kombineres med chloridioner (CL⁻) for at danne magnesiumchlorid (MGCL₂).
Kobberens inaktivitet
* kobber + saltsyre (HCL) → Ingen reaktion
Kobber er mindre reaktiv end brint. Det kan ikke fortrænge brint fra saltsyre. Som et resultat forekommer der ingen reaktion.
resume
Magnesium kan reagere med saltsyre, fordi det er mere reaktivt end brint og kan fortrænge det. Kobber, der er mindre reaktiv, kan ikke fortrænge brint og reagerer derfor ikke med saltsyre.
Fortæl mig, hvis du gerne vil have yderligere forklaring!
 Varme artikler
Varme artikler
-
 Kunstig intelligens fremskynder fotodynamiske simuleringerIllustration til undersøgelsen, som dukkede op på et af forsiderne til Kemisk videnskab:Kunstige neurale netværk hjælper med drastisk at accelerere simuleringer af fotoinducerede processer. Kredit:Jul
Kunstig intelligens fremskynder fotodynamiske simuleringerIllustration til undersøgelsen, som dukkede op på et af forsiderne til Kemisk videnskab:Kunstige neurale netværk hjælper med drastisk at accelerere simuleringer af fotoinducerede processer. Kredit:Jul -
 Mystiske cellulære dråber kommer i fokusIndividuelle proteinmolekyler, der udgør kondensatet, fremhæves med farve. Kredit:Han-Yi Chou, University of Illinois, Urbana-Champaign Verden inde i den menneskelige celle er blevet en smule mere
Mystiske cellulære dråber kommer i fokusIndividuelle proteinmolekyler, der udgør kondensatet, fremhæves med farve. Kredit:Han-Yi Chou, University of Illinois, Urbana-Champaign Verden inde i den menneskelige celle er blevet en smule mere -
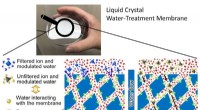 Meget selektive membraner:Forskere opdager, hvordan vand kan påvirke sin egen filtreringDen subnanoporøse væske-krystallinske vandbehandlingsmembran kan være meget selektiv med hensyn til, hvad den lader passere igennem. Kredit:Kato og Harada et al. Membraner med mikroskopiske porer
Meget selektive membraner:Forskere opdager, hvordan vand kan påvirke sin egen filtreringDen subnanoporøse væske-krystallinske vandbehandlingsmembran kan være meget selektiv med hensyn til, hvad den lader passere igennem. Kredit:Kato og Harada et al. Membraner med mikroskopiske porer -
 Bouncende bobler ryster emulsionsundersøgelserHøjhastighedskamera snapshots og simuleringer af bobler, der hopper fra vand-luft-grænseflader, kan bruges til at detektere spormængder af forurenende stoffer. Kredit:Ivan Vakarelski Nogle af de h
Bouncende bobler ryster emulsionsundersøgelserHøjhastighedskamera snapshots og simuleringer af bobler, der hopper fra vand-luft-grænseflader, kan bruges til at detektere spormængder af forurenende stoffer. Kredit:Ivan Vakarelski Nogle af de h
- Uventet regn på solen forbinder to solmysterier
- 3D-sporing af enkeltmolekyler inde i celler
- Er det sikkert? Hvorfor nogle dyr frygter at bruge krydsninger af vilde dyr
- Sådan beregnes hastigheden af to forskellige remskiver
- Sådan virker benzin
- Journey of a skull:Hvordan en enkelt menneskelig kranium endte alene i hulen Italien


