Hvorfor er HF polær kovalent ikke en ionisk forbindelse, skønt forskellen i elektronegativiteter 1.9?
* størrelse på fluoratomet: Fluor er meget lille og har en høj elektronegativitet. Dette betyder, at dens kerne kraftigt kan tiltrække det delte elektronpar i bindingen. Imidlertid er fluor også meget elektronegativ, hvilket gør det vanskeligt at miste en elektron og blive en anion.
* Hydrogen's unikke opførsel: Mens brint ikke er særlig elektronegativ, har det en stærk tendens til at danne en enkelt kovalent binding. Dette gør det mindre sandsynligt, at det mister sin elektron fuldstændigt og bliver en kation.
* obligationsstyrke: Bindingen mellem brint og fluor er overraskende stærk på grund af den lille størrelse og høje elektronegativitet af fluor. Denne stærke binding gør det mindre sandsynligt at overføre elektroner fuldstændigt.
hvad gør HF polær kovalent?
Mens det delte elektronpar trækkes stærkt mod fluoratomet, overføres det ikke helt. Dette skaber en delvis negativ ladning På fluoratomet (Δ-) og A delvis positiv ladning på hydrogenatomet (δ+). Denne ujævne fordeling af ladning gør molekylet polær.
Nøglepunkt: Selvom elektronegativitetsforskellen er betydelig, fører samspillet mellem faktorer som størrelse, bindingsstyrke og Hydrogen's opførsel til dannelse af en stærk, polær kovalent binding i HF.
 Varme artikler
Varme artikler
-
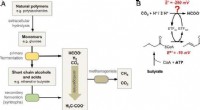 Afgørende trin identificeret i omdannelsen af biomasse til metanKredit:DOI:10.1073/pnas.2111682118 Mikrobiel produktion af metan fra organisk materiale er en væsentlig proces i det globale kulstofkredsløb og en vigtig kilde til vedvarende energi. Denne naturli
Afgørende trin identificeret i omdannelsen af biomasse til metanKredit:DOI:10.1073/pnas.2111682118 Mikrobiel produktion af metan fra organisk materiale er en væsentlig proces i det globale kulstofkredsløb og en vigtig kilde til vedvarende energi. Denne naturli -
 Hvordan en vietnamesisk rå svinekødssnack kunne hjælpe os med at holde maden frisk, naturligtVietnamesisk fermenteret svinekødssnack, Nem Chua. Kredit:RMIT University En traditionel vietnamesisk kødsnack kunne indeholde nøglen til at udvikle et sikkert og naturligt fødevarekonserveringsmi
Hvordan en vietnamesisk rå svinekødssnack kunne hjælpe os med at holde maden frisk, naturligtVietnamesisk fermenteret svinekødssnack, Nem Chua. Kredit:RMIT University En traditionel vietnamesisk kødsnack kunne indeholde nøglen til at udvikle et sikkert og naturligt fødevarekonserveringsmi -
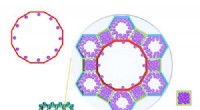 Realtidsanalyse af MOF-adsorptionsadfærdSkematisk illustration af molekyler adsorberet på metalorganiske rammer med forskellige porer af forskellige strukturer, hvor In-situ røntgenkrystallografi er blevet udviklet til at klassificere hver
Realtidsanalyse af MOF-adsorptionsadfærdSkematisk illustration af molekyler adsorberet på metalorganiske rammer med forskellige porer af forskellige strukturer, hvor In-situ røntgenkrystallografi er blevet udviklet til at klassificere hver -
 Forskere udvikler enzym fremstillet af landbrugsaffald til brug som vaskemiddelDr. Pattanathu Rahman. Kredit:University of Portsmouth Et internationalt forskerhold har udviklet et enzym fremstillet af landbrugsaffald, der kunne bruges som et vigtigt tilsætningsstof i vaskemi
Forskere udvikler enzym fremstillet af landbrugsaffald til brug som vaskemiddelDr. Pattanathu Rahman. Kredit:University of Portsmouth Et internationalt forskerhold har udviklet et enzym fremstillet af landbrugsaffald, der kunne bruges som et vigtigt tilsætningsstof i vaskemi
- Hvordan opretholder kroppen et stabilt pH-niveau?
- Regntiden har en tendens til at begynde tidligere i det nordlige Centralasien
- Hvordan dannes mineraler af magma og lava?
- Flere fragmenter fra 1952 styrt i Alaska fundet i gletsjer
- Amerikanske prognosemænd:Her kommer endnu en varmere sommer end normal
- Mine håndværk til Mars


