Bestem det teoritiske udbytte af H2S i mol, hvis 4,0 mol Al2S3 og H2O reageres?
1. Afbalanceret kemisk ligning:
Den afbalancerede kemiske ligning for reaktionen er:
Al₂s₃ + 6H₂O → 2Al (OH) ₃ + 3H₂S
2. Molforhold:
Fra den afbalancerede ligning ser vi, at 1 mol Al₂s₃ reagerer for at producere 3 mol H₂S.
3. Teoretisk udbytteberegning:
Da vi har 4,0 mol Al₂s₃, kan vi bruge molforholdet til at beregne det teoretiske udbytte af H₂s:
(4,0 mol al₂s₃) × (3 mol H₂s / 1 mol al₂s₃) = 12 mol H₂s
Derfor er det teoretiske udbytte af H₂s 12 mol.
 Varme artikler
Varme artikler
-
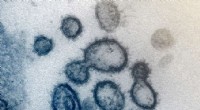 Nyt værktøj trækker undvigende COVID-19-markør fra menneskeblodDette transmissionselektronmikroskopbillede viser SARS-CoV-2 - også kendt som 2019-nCoV, virussen, der forårsager COVID-19 - isoleret fra en patient i USA. Viruspartikler er vist, der dukker op fra ov
Nyt værktøj trækker undvigende COVID-19-markør fra menneskeblodDette transmissionselektronmikroskopbillede viser SARS-CoV-2 - også kendt som 2019-nCoV, virussen, der forårsager COVID-19 - isoleret fra en patient i USA. Viruspartikler er vist, der dukker op fra ov -
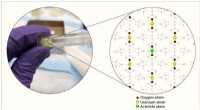 Undersøgelse afslører et-trins strategi for genanvendelse af brugt nukleart brændselEt-trins kemisk reaktion foreskrevet i undersøgelsen fører til dannelsen af krystaller, der indeholder uran (gulfyldte cirkler) og små mængder af andre resterende brændstofelementer (grønfyldte cirk
Undersøgelse afslører et-trins strategi for genanvendelse af brugt nukleart brændselEt-trins kemisk reaktion foreskrevet i undersøgelsen fører til dannelsen af krystaller, der indeholder uran (gulfyldte cirkler) og små mængder af andre resterende brændstofelementer (grønfyldte cirk -
 Ny metode til konstruktion af metaboliske vejeKredit:CC0 Public Domain Celler er utroligt dygtige til at skabe komplekse molekyler, ligesom terapi, og kan gøre så meget bedre end mange af vores bedste fabrikker. Syntetiske biologer søger at
Ny metode til konstruktion af metaboliske vejeKredit:CC0 Public Domain Celler er utroligt dygtige til at skabe komplekse molekyler, ligesom terapi, og kan gøre så meget bedre end mange af vores bedste fabrikker. Syntetiske biologer søger at -
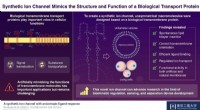 Forskere syntetiserer nye kunstige molekyler, der efterligner et cellemembranproteinEn usymmetrisk molekylær struktur muliggør orienteret indsættelse af den syntetiske amfifil til et dobbeltlag ved tilsætning til en præformet membran. Kompleksation med en ligand tilskynder iontranspo
Forskere syntetiserer nye kunstige molekyler, der efterligner et cellemembranproteinEn usymmetrisk molekylær struktur muliggør orienteret indsættelse af den syntetiske amfifil til et dobbeltlag ved tilsætning til en præformet membran. Kompleksation med en ligand tilskynder iontranspo
- Brasiliansk nød -effekt hjælper med at forklare, hvordan floder modstår erosion, team finder
- Er Santa Fe nord eller syd for den tropiske Stenbukken?
- Er det et efterforskningsprojekt at lave en mini personlig elektrisk fan?
- Kina udgiver verdens første geologiske måneatlas i høj opløsning
- Lag brint ud af den blå luft
- Sådan løses lineære ligninger


