Hvad er den samlede spænding for en redoxreaktion med halvreaktioner Mg S- Mg2 plus 2e- og Cu2 Cu S?
1. Identificer halvreaktionerne:
* Oxidation: Mg (s) → mg²⁺ (aq) + 2e⁻
* reduktion: Cu²⁺ (aq) + 2e⁻ → cu (s)
2. Slå op på standardreduktionspotentialer:
Du skal finde standard reduktionspotentialer (E °) for hver halvreaktion. Disse værdier findes typisk i tabeller.
* E ° (mg²⁺/mg) =-2,37 V
* E ° (cu²⁺/cu) =+0,34 V
3. Bestem det samlede cellepotentiale:
Det samlede cellepotentiale (E ° celle) beregnes som:
E ° celle =E ° (reduktion) - E ° (oxidation)
* Da magnesiumhalvreaktionen er oxidationen (elektroner går tabt), er vi nødt til at vende tegnet på dets reduktionspotentiale.
E ° celle =+0,34 V - (-2,37 V)
E ° celle =+2,71 V
Derfor er den samlede spænding for redoxreaktionen +2,71 v.
Vigtige noter:
* spontane reaktioner: Et positivt cellepotentiale indikerer, at reaktionen er spontan under standardbetingelser (25 ° C, 1 ATM -tryk, 1 m koncentration).
* ikke-standardforhold: Hvis reaktionen ikke forekommer under standardbetingelser, skal du bruge Nernst -ligningen til at beregne cellepotentialet.
Sidste artikelEr pH 4 stærkere end PH3?
Næste artikelBestem det teoritiske udbytte af H2S i mol, hvis 4,0 mol Al2S3 og H2O reageres?
 Varme artikler
Varme artikler
-
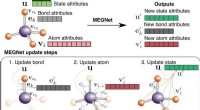 Ingeniører bruger grafnetværk til nøjagtigt at forudsige egenskaber af molekyler og krystallerSkematisk illustration af MEGNet-modeller. Kredit:Chi Chen/Materials Virtual Lab Nanoingeniører ved University of California San Diego har udviklet nye deep learning-modeller, der præcist kan foru
Ingeniører bruger grafnetværk til nøjagtigt at forudsige egenskaber af molekyler og krystallerSkematisk illustration af MEGNet-modeller. Kredit:Chi Chen/Materials Virtual Lab Nanoingeniører ved University of California San Diego har udviklet nye deep learning-modeller, der præcist kan foru -
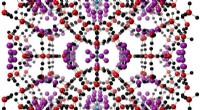 CO2 clathrate hydrat egenskaberFigur 1:Krystalstruktur af et CO2-klatrathydrat. Burstrukturen er dannet ud fra interaktionen af CO2-gas med vandmolekyler i is (rød og sort:ilt- og brintatomer, henholdsvis). CO2-molekyler (blå og
CO2 clathrate hydrat egenskaberFigur 1:Krystalstruktur af et CO2-klatrathydrat. Burstrukturen er dannet ud fra interaktionen af CO2-gas med vandmolekyler i is (rød og sort:ilt- og brintatomer, henholdsvis). CO2-molekyler (blå og -
 Forskere kaster nyt lys over molekylær adfærdKredit:CC0 Public Domain Forskere ved Heriot-Watt University har udviklet et nyt eksperiment, der har afsløret aldrig før set molekylær adfærd. Et team af forskere ledet af professor Matt Costen
Forskere kaster nyt lys over molekylær adfærdKredit:CC0 Public Domain Forskere ved Heriot-Watt University har udviklet et nyt eksperiment, der har afsløret aldrig før set molekylær adfærd. Et team af forskere ledet af professor Matt Costen -
 Picosecond-elektronoverførsel i peptider kan hjælpe energiteknologierDet forlængede peptid (øverst) medierer ikke ladningsoverførsel (detekterbar ladningsoverførsel)/ Det foldede peptid (nederst) medierer picosecond ladningsoverførsel langs hydrogenbindingerne mellem d
Picosecond-elektronoverførsel i peptider kan hjælpe energiteknologierDet forlængede peptid (øverst) medierer ikke ladningsoverførsel (detekterbar ladningsoverførsel)/ Det foldede peptid (nederst) medierer picosecond ladningsoverførsel langs hydrogenbindingerne mellem d


