Hvad er hybridiseringen af SIH4?
* silicium (SI) har 4 valenselektroner.
* hvert brint (H) atom har 1 valenselektron.
* For at danne SIH4 skal silicium danne 4 enkeltbindinger med 4 hydrogenatomer.
For at imødekomme disse 4 obligationer har silicium behov for 4 orbitaler. Det opnår dette ved at hybridisere sine 3s orbital og dens tre 3p orbitaler, der danner fire ækvivalente SP3 -hybrid -orbitaler. Hver af disse hybrid -orbitaler overlapper derefter med 1s orbital af et hydrogenatom for at danne en Sigma -binding.
Derfor er hybridiseringen af SIH4 SP3, hvilket resulterer i en tetrahedral molekylær geometri.
Sidste artikelEr aluminiumssodavand nedbrydningstid?
Næste artikelHvad er forskellen mellem anvendt kemi og industriel kemi?
 Varme artikler
Varme artikler
-
 Havvand giver de første gram gulkage:Garnlignende materiale opsamler den største mængde uran til …Dette første gram gulkage blev fremstillet af uran fanget fra havvand med modificeret garn. Chien Wai og kolleger hos LCW Supercritical Technologies producerede den gule kage, en pulveriseret form for
Havvand giver de første gram gulkage:Garnlignende materiale opsamler den største mængde uran til …Dette første gram gulkage blev fremstillet af uran fanget fra havvand med modificeret garn. Chien Wai og kolleger hos LCW Supercritical Technologies producerede den gule kage, en pulveriseret form for -
 Vejskilte for immunforsvarscellerKredit:CC0 Public Domain Organismer bliver konstant invaderet af patogener såsom vira. Vores immunsystem går i gang for at bekæmpe disse patogener med det samme. Det medfødte uspecifikke immunrespo
Vejskilte for immunforsvarscellerKredit:CC0 Public Domain Organismer bliver konstant invaderet af patogener såsom vira. Vores immunsystem går i gang for at bekæmpe disse patogener med det samme. Det medfødte uspecifikke immunrespo -
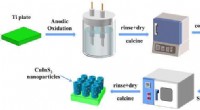 CuInS2/TiO2-fotoanodekompositter klarer sig godt i foto-induceret katodisk beskyttelseGrafisk abstrakt. Kredit:Journal of Materials Science &Technology (2022). DOI:10.1016/j.jmst.2022.02.011 Fotogenereret katodisk beskyttelsesteknologi som en værdifuld gren af fotokatalyse og foto
CuInS2/TiO2-fotoanodekompositter klarer sig godt i foto-induceret katodisk beskyttelseGrafisk abstrakt. Kredit:Journal of Materials Science &Technology (2022). DOI:10.1016/j.jmst.2022.02.011 Fotogenereret katodisk beskyttelsesteknologi som en værdifuld gren af fotokatalyse og foto -
 Kirurgi i en pille en potentiel behandling for diabetesOperation i en pille i tarmen. Kredit:Brigham and Womens Hospital og Randal Mckenzie I løbet af det sidste årti, bariatriske kirurger har gjort fremskridt med at udføre vægttabskirurgi, der ikke k
Kirurgi i en pille en potentiel behandling for diabetesOperation i en pille i tarmen. Kredit:Brigham and Womens Hospital og Randal Mckenzie I løbet af det sidste årti, bariatriske kirurger har gjort fremskridt med at udføre vægttabskirurgi, der ikke k
- Sådan beregnes Debye Length
- Metode til at belyse egenskaber ved biologiske væv i billeder med lav eksponering
- Hvordan dannes en løsning?
- Hvordan vævsgeometri påvirker bevægelsen af celler gennem kroppen
- Hvilket eksperiment kan du gøre for at vise, om en plastikstang har ændret sig eller ej?
- Hvad spiser paramecium?


