Er fosfor trihydridionisk eller kovalent?
* Elektronegativitetsforskel: Fosfor (P) og brint (H) har relativt ens elektronegativitetsværdier. Forskellen er ikke stor nok til at skabe en betydelig ionisk karakter i bindingen.
* Deling af elektroner: I pH₃ deler fosfor sine elektroner med de tre brintatomer til dannelse af kovalente bindinger. Denne deling af elektroner resulterer i et stabilt molekyle.
Vigtig note: Mens bindingen mellem fosfor og brint primært er kovalent, har den en lille grad af polaritet på grund af den lette elektronegativitetsforskel. Dette betyder, at phosphoratomet har en lidt negativ ladning, og brintatomerne har en lidt positiv ladning.
 Varme artikler
Varme artikler
-
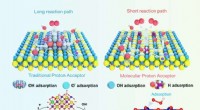 Designstrategi på molekylært niveau kan være nøglen til at øge kommerciel brintproduktionSammenligning mellem reaktionsmekanismerne i et hybridsystem med en konventionel heterostruktur og enkeltfasesystemet med protonacceptorer på molekylært niveau udviklet af forskerne. Kredit:Nanjing Un
Designstrategi på molekylært niveau kan være nøglen til at øge kommerciel brintproduktionSammenligning mellem reaktionsmekanismerne i et hybridsystem med en konventionel heterostruktur og enkeltfasesystemet med protonacceptorer på molekylært niveau udviklet af forskerne. Kredit:Nanjing Un -
 Ingeniører laver en simpel test, der kan måle stresshormoner i sved, blod, urin eller spytUniversity of Cincinnati forskningsassistent Shima Dalirirad undersøger en maskine, der udskriver teststrimler i UCs Nanoelectronics Laboratory. Kredit:Andrew Higley/UC Creative Services Stress ka
Ingeniører laver en simpel test, der kan måle stresshormoner i sved, blod, urin eller spytUniversity of Cincinnati forskningsassistent Shima Dalirirad undersøger en maskine, der udskriver teststrimler i UCs Nanoelectronics Laboratory. Kredit:Andrew Higley/UC Creative Services Stress ka -
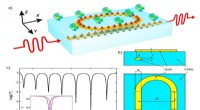 Blod og sved:Bærbare medicinske sensorer vil få et stort følsomhedsforøgelseBiosensor layout (en, c). Bølgelederen er inde i det dielektriske substrat. Resonatoren, realiseret som en ringbølgeleder, er placeret ved grænsefladen mellem det dielektriske materiale og den biologi
Blod og sved:Bærbare medicinske sensorer vil få et stort følsomhedsforøgelseBiosensor layout (en, c). Bølgelederen er inde i det dielektriske substrat. Resonatoren, realiseret som en ringbølgeleder, er placeret ved grænsefladen mellem det dielektriske materiale og den biologi -
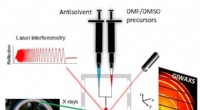 Røntgenstråler afslører in situ krystalvækst af blyfrie perovskit solpanelmaterialerEt skema over den eksperimentelle opsætning, der bruges til at undersøge den strukturelle dannelse af perovskites tynde film under spinbelægning. Kredit:G.Portale, University of Groningen Blybaser
Røntgenstråler afslører in situ krystalvækst af blyfrie perovskit solpanelmaterialerEt skema over den eksperimentelle opsætning, der bruges til at undersøge den strukturelle dannelse af perovskites tynde film under spinbelægning. Kredit:G.Portale, University of Groningen Blybaser
- Billede:Glacial efterskælv gyder Antarktis isbjerg
- AI-modeller forudsiger henfaldstilstande og halveringstider for supertunge kerner med hidtil uset nø…
- Hvilket dyr ville være på 2. trofisk niveau?
- Hvad er det største lag af jordoverfladen?
- Klimaeffekterne vil koste verden $ 7,9 billioner i 2050
- Hvad er den faktiske dato uden springår og besparelser i dagslys?


