En række hydrofobe sidekæder samles sammen som proteinfoldninger i en vandig opløsning og stabiliseres af?
Her er en sammenbrud:
* Hydrofob effekt: Vandmolekyler er polære og danner stærke brintbindinger med hinanden. Ikke -polære molekyler (som hydrofobe sidekæder) forstyrrer disse hydrogenbindinger og er derfor ugunstige i et vandigt miljø. For at minimere denne forstyrrelse klynger hydrofobe sidekæder sammen i det indre af proteinet væk fra vandet.
* stabilisering: Denne klynge er ikke drevet af en direkte tiltrækning mellem hydrofobe sidekæder. I stedet er det en konsekvens af den øgede entropi (lidelse) af de omgivende vandmolekyler, når de hydrofobe grupper begraves i proteinet. Denne stigning i entropi driver foldningsprocessen og stabiliserer den foldede proteinstruktur.
I resuméet drives hydrofobe sidekæder i et protein til at mødes i et vandigt miljø for at minimere forstyrrelsen af vandmolekyler og øge systemets samlede entropi. Dette er en vigtig drivkraft i proteinfoldning.
 Varme artikler
Varme artikler
-
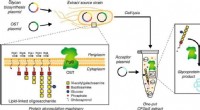 Bioingeniører skaber vej til personlig medicinSkematisk af enkelt-pot CFGpS-teknologi. Glycoengineered E. coli, der er modificeret med (i) genomiske mutationer, der gavner glykosyleringsreaktioner og (ii) plasmid -DNA til fremstilling af essentie
Bioingeniører skaber vej til personlig medicinSkematisk af enkelt-pot CFGpS-teknologi. Glycoengineered E. coli, der er modificeret med (i) genomiske mutationer, der gavner glykosyleringsreaktioner og (ii) plasmid -DNA til fremstilling af essentie -
 Redesigner håndsprit og donerer 7, 000 gallons til at bekæmpe COVID-19Håndsprit reddet af ethanol. Et velgørende initiativ kørte for at forhindre håndsprit i at løbe kritisk lavt over hele landet. Kredit:Georgia Tech/Christopher Moore Så mange mennesker, Seth Marder
Redesigner håndsprit og donerer 7, 000 gallons til at bekæmpe COVID-19Håndsprit reddet af ethanol. Et velgørende initiativ kørte for at forhindre håndsprit i at løbe kritisk lavt over hele landet. Kredit:Georgia Tech/Christopher Moore Så mange mennesker, Seth Marder -
 Atomisk opfattelse af naturens fantastiske molekylære maskiner på arbejdeMetoden hit and return (HARE) forenkler optagelse af snapshot-film af biomolekyler på arbejdet. Kredit:J. M. Harms, MPSD Forskere fra MPSDs Institut for Atomically Resolved Dynamics ved Center for
Atomisk opfattelse af naturens fantastiske molekylære maskiner på arbejdeMetoden hit and return (HARE) forenkler optagelse af snapshot-film af biomolekyler på arbejdet. Kredit:J. M. Harms, MPSD Forskere fra MPSDs Institut for Atomically Resolved Dynamics ved Center for -
 Syntetisering af et superatom:Åbning af døre til deres anvendelse som erstatning for elementære a…Baseret på dendrimer-skabelonmetoden, klynger bestående af 3, 12, 13 og et andet antal atomer er blevet syntetiseret. Den halogenlignende superatomare natur af Ga13 blev strukturelt og elektrokemisk o
Syntetisering af et superatom:Åbning af døre til deres anvendelse som erstatning for elementære a…Baseret på dendrimer-skabelonmetoden, klynger bestående af 3, 12, 13 og et andet antal atomer er blevet syntetiseret. Den halogenlignende superatomare natur af Ga13 blev strukturelt og elektrokemisk o
- Ville eddike påvirke det frysepunkt for vand?
- Undersøgelse giver ny indsigt om overfladen og strukturen af asteroide Bennu
- Sådan træner Large Hadron Collider sine magneter
- Eksperimenter sætter tvivl om, hvordan Jorden blev dannet
- Hvad er H3O plus -koncentrationen i en opløsning, der er 100 gange mindre sur end en, der har PH på…
- 'Vi har lige opdaget det umulige':Hvordan gigantiske babygalakser ryster op i vores forståelse af d…


